Operative metoder som benyttes ved brystkreft:
- Diagnostisk biopsi
- Brystbevarende kirurgi (BCT) med eller uten onkoplastisk korreksjon (OBCS)
- Ablatio mammae (mastektomi) med eller uten primær rekonstruksjon
- Vaktpostlymfeknutebiopsi (SNB)
- Aksilledisseksjon (AD)
Ved operativ behandling av maligne forandringer i brystvevet skal det tas hensyn til så vel kirurgiske, onkologiske, samt kosmetiske forhold. Onkologiske prinsipper prioriteres over kosmetiske hensyn. Kosmetiske problemer i forbindelse med operasjon for brystkreft dreier seg i første omgang om hudoverskudd omkring arret etter mastektomi, deformering av brystet etter brystbevarende kirurgi samt skjemmende arr. Planlegging og utførelse av diagnostiske eller terapeutiske inngrep må derfor tilstrebe å unngå slike problemer.
Gjennom vurdering av den individuelle pasients brystkonfigurasjon som bryststørrelse, ptosegrad og komorbiditet må inngrepet planlegges ut fra grunnprinsipper og tekniske anbefalinger.
I tverrfaglig møte der kirurgi planlegges bør følgende tas med i betraktning:
- Tumorlokalisasjon og størrelse
Store eksisjoner er mulig i øvre laterale kvadrant uten behov for større korreksjoner. Risiko for asymmetri og deformitet av brystet øker ved selv mindre eksisjoner i de andre kvadrantene uten bruk av onkoplastiske teknikker. Prosent eksidert brystvolum er den viktigste faktoren av betydning for kosmetisk utseende (Chan et al., 2010; Cochrane et al., 2003). - Brystkjerteltetthet (densitet)
Kjertel med økt tetthet krever i høyere grad mobilisering og lukning av kaviteten. Ved redusert tetthet skal en være forsiktig med mobilisering av vev grunnet risiko for fettvevsnekrose (Clough et al., 2003).
Diagnostisk biopsi
Indisert der hvor man ikke har preoperativ diagnose ved hjelp av FNAC, sylinderbiopsi eller vakumbiopsi. Se kapittel Diagnostisk åpen biopsi/merkebiopsi.
Teknikk
Følger teknikk som ved BCT der en tilstreber at snittet ikke kommer i konflikt med et eventuelt senere ablatio-snitt eller OBCS. Snittføring periareolært gir ofte et godt kosmetisk resultat. Som ved brystbevarende operasjon, skal tumorkaviteten alltid klipses, men antall klips kan være mindre der sårhulen er liten og/eller mistanken om cancer/DCIS er liten. Det bør alltid benyttes minst 5 klips slik at dorsalt, medialt, lateralt, kranialt og kaudalt i sårhulen er definert.MR kompatible klips skal benyttes.
Palpabel tumor: Bør om mulig gjøres ved at tumor fjernes fullstendig.
Merkebiopsi er aktuelt ved ikke-palpable malignitetssuspekte mikroforkalkninger eller ikke-palpabel malignitetssuspekt lesjon hvor man ikke har stilt klar diagnose ved vakumbiopsi, sylinderbiopsi eller FNAC. Merking gjøres preoperativt enten ultralyd- eller stereotaktisk veiledet. Preparatet må billedmessig verifiseres, kfr. utredningskapitlet.
Brystbevarende kirurgi
Målsetning for brystbevarende kirurgi
- Samme overlevelse som ved ablatio
- God lokal kontroll ved å sikre lav risiko for ipsilateralt residiv (< 1 % per år)
- Kosmetisk resultat må forventes å bli like godt og ofte bedre enn ablatio fulgt av rekonstruksjon
- Brystbevarende kirurgi foretrekkes der det er teknisk mulig og forholdene ligger til rette for det (de Boniface et al., 2021)
Kontraindikasjoner / relative kontraindikasjoner mot brystbevarende kirurgi
(American College of Radiology, 2007; Bartelink et al., 2001; Cabioglu et al., 2005; Clarke et al., 2005; Fisher et al., 2002; Houssami et al., 2010; Larson et al., 2018; Litiere et al., 2012; Veronesi et al., 2002; Veronesi et al., 1995)
Absolutte:
- Hos gravide der strålebehandling (etter eventuelt brystbevarende inngrep) ikke kan utsettes til etter avsluttet svangerskap
- Diffuse malignitetssuspekte mikroforkalkninger som omfatter flere segmenter av brystet. Utbredelsen bør verifiseres histologisk preoperativt.
- Ikke frie reseksjonsrender der videre rereseksjon ikke er mulig
- Der strålebehandling ikke lar seg gjennomføre (f.eks alvorlig hjerte-/lungesykdom eller thoraxmalformasjon)
- Lokalavansert situasjon som tilsier bruk av neoadjuvant systemisk behandling (kfr Aksillemetastase(r) fra brystkreft uten påvist primærtumor i bryst)
Relative:
- Aktiv bindevevssykdom som affiserer hud (f.eks. sklerodermi og lupus)
- Stor tumor i et lite bryst (se avsnittet lengre ned om onkoplastisk kirurgi, samt kapittel Lokalavansert brystkreft)
- Kjent mutasjon i BRCA 1 eller 2 (utgjør 3–5 % av all brystkreft). Disse pasientene har en økt risiko for å få et ipsilateralt recidiv og kontralateral brystkreft. Retrospektive studier har vist en overlevelsesgevinst ved å gjøre bilateral mastektomi hos pasienter med BRCA 1 og 2 mutasjon (Metcalfe et al., 2014; Valachis et al., 2014). Hos mange pasienter kan det være hensiktsmessig å gjøre et brystbevarende inngrep i første omgang og det endelige profylaktiske inngrepet etter evt. adjuvant kjemoterapi og før evt. strålebehandling.
- Tidligere strålebehandling mot bryst eller brystvegg etter brystbevarende kirurgi vanskeliggjør ny brystbevarende kirurgi, men kfr. kapittel Risikoorganer.
- Mastektomi er førstevalg hos kvinner med brystkreft og kimbane genfeil i TP53 (Tung et al., 2020). Strålebehandling bør unngås hos disse pasientene på grunn av økt risiko for stråleindusert kreft.
Neoadjuvant behandling og brystbevarende inngrep
Der tumor er så stor i forhold til brystets størrelse at et brystbevarende inngrep med eller uten OBCS, ikke lar seg gjøre, evt. at tumor er beliggende i ugunstige lokalisasjoner av brystet, kan neoadjuvant behandling (kjemoterapi eller endokrin behandling) bidra til å legge forholdene til rette for et brystbevarende inngrep dersom det oppnås en tilstrekkelig reduksjon i tumor¬størrelsen (Mieog et al., 2007). Respons på neoadjuvant behandling er størst ved trippel negative og HER2 positive svulster (Houssami et al., 2012).
Spesielle forhold for DCIS
Det oppfattes ikke å være grunnlag for å sette en øvre grense for utbredelse av DCIS for at BCT kan gjennomføres så lenge det ligger til rette for radikal eksisjon med frie marginer og brystets størrelse tillater dette (Bijker et al., 2013; Collins et al., 2013; Rakovitch et al., 2013).
Makromasti
Stor bryststørrelse alene er nå svært sjelden årsak til at postoperativ strålebehandling ikke kan gis. Dersom det likevel anses vanskelig, bør det foretas en reduksjonsplastikk samtidig med det brystbevarende inngrepet med mindre det foreligger kontraindikasjoner. Der det gjøres et brystbevarende inngrep som medfører en stor volumasymmetri i forhold til motsatt bryst, bør et symmetriserende inngrep i forbindelse med primærinngrepet tilstrebes.
Konvensjonell brystbevarende operasjon (BCT)
Teknikk
Periareolære snitt er å foretrekke. Det er viktig å legge snittet slik at eventuelt senere ablatio snittføring vil omfatte dette. Vanligvis fjernes vevet mellom hud og pectoralismuskelen. Ved hudnær tumor kan det være nødvendig å fjerne huden over tumor. Preparatet orienteres i enighet med patologen. Tusjmerking peroperativt av kirurg kan være en fordel (Landercasper et al., 2015).
Reseksjonen skal være fullstendig og inngrepet må planlegges med tanke på å oppnå en tumorfri margin.
For å underlette strålebehandlingen skal sårhulen alltid klipses, men antall klips kan være mindre der sårhulen er liten og/eller mistanken om cancer/DCIS er liten. Det bør alltid benyttes minst 5 klips slik at dorsale, mediale, laterale, kraniale og kaudale del av sårhulen er definert.
Onkoplastisk brystkirurgi (OBCS)
Onkoplastisk brystkirurgi (OBCS) innebærer bruk av plastikkirurgiske teknikker ved fjerning av tumor for å opprettholde brystets form og ofte også volum. I videste forstand gjelder det også primær rekonstruksjon med implantater, men det er vanlig å snevre inn begrepet OBCS til remodellering/rekonstruksjon av brystet i forbindelse med et brystbevarende inngrep.
Der hvor tumorstørrelse relatert til brystets størrelse, tumorlokalisasjon eller andre forhold taler for at det ikke kan oppnås et tilfredsstillende kosmetisk resultat ved et konvensjonelt brystbevarende inngrep, bør onkoplastiske teknikker vurderes. I tillegg til mulighet for et bedre kosmetisk resultat, vil bruk av OBCS kunne redusere behov for reeksisjoner og øke andelen som kan få et brystbevarende inngrep uten at det blir flere postoperative komplikasjoner eller forsinket oppstart av adjuvant behandling (Campbell et al., 2017). Onkoplastisk kirurgi kan utføres med samme onkologiske sikkerhet som konvensjonell BCT og ablatio (De La Cruz et al., 2016; Mansell et al., 2017). Studier som har sett på lokalt tilbakefall og brystkreftspesifikk overlevelse etter OBCS har dog begrensninger i form av kort observasjonstid og suboptimalt sammenligningsgrunnlag mht tumorkarakteristika og manglende informasjon om boostbestråling er gitt. OBCS kan pga vevs-rearrangering medføre vansker med sikker lokalisering av primær tumorseng som anbefales bestrålt med boost hos pasienter <40(50) år/og eller ved ufrie reseksjonsrender (se for øvrig kapittel "Strålebehandling ved lokalisert sykdom"). Vurdering av om BCT og evt. OBCS kan være aktuelt, bør gjøres i et MDT møte og vurderes klinisk av kirurg med kompetanse på OBCS.
På generelt grunnlag vil fjerning av mer enn ca. 15 % av brystkjertelvevet gi et dårlig kosmetisk resultat dersom ikke onkoplastiske teknikker benyttes. Er tumor lokalisert i nedre kvadranter eller i øvre mediale kvadrant, kan OBCS også være indisert ved eksisjon av et volum brystkjertelvev mindre enn 15 % (Chan et al., 2010). Se figur 5.1 for vurdering av tumorstørrelse mot brystvolum, såkalt «tumor to breast size ratio». Ulike prosedyrer er aktuelle ved ulike bryststørrelser.
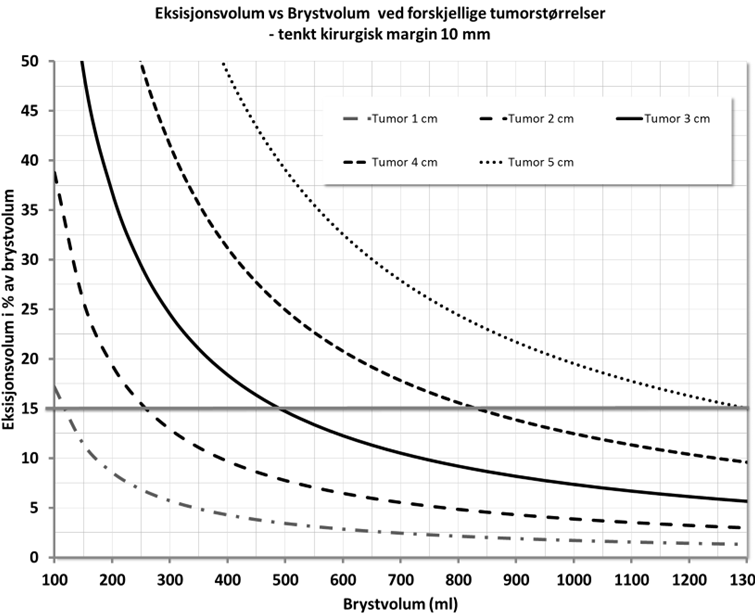
Operatør må være kjent med at boostområdet kan bli vanskeligere å identifisere ved stråleplanleggingen. Videre kan området for boostbestråling øke i størrelse, noe som kan medføre økt risiko for redusert kosmetisk resultat, fibrose og/eller økt stråledose på underliggende organer. Pasienten må informeres godt om inngrepet og at det ved ufrie reseksjonskanter, kan bli nødvendig å gjøre en mastektomi dersom rereseksjon ikke er mulig. Videre må pasientene informeres om at det kan være nødvendig med et kontralateralt inngrep dersom man ønsker symmetri. Tidspunkt for et slikt inngrep må disku¬teres med pasienten. Det kan være praktisk å gjøre det samtidig med primærkirurgien, men det kan også være grunn for å avvente et slikt symmetriserende inngrep til noen tid etter strålebehandlingen da denne kan påvirke brystets volum.
Det bør gjøres fotodokumentasjon til journal av overkroppen til alle pasienter som opereres med BCT og spesielt av pasienter som tilbys OBCS. Bilder tas av stående pasient i 5 projek¬sjoner (front, skrått og side bilateralt) med tumorområdet inntegnet på brystet før og et bilde etter inngrepet.
Med tanke på postoperativ strålebehandling er det spesielt viktig å huske klips i sårhulen (se avsnittet over om Brystbevarende kirurgi). Dersom det benyttes klips for hemostase i brystet, må det beskrives i operasjons¬beskrivelsen slik at det ikke skaper unødvendige vansker ved innstilling av strålefelt. En detaljert beskrivelse av det kirurgiske inngrepet er viktig. Operasjonspreparatet må orienteres for histopatologisk undersøkelse og tusjmerking ved kirurg anbefales (Landercasper et al., 2015).
De vanligste teknikkene ved OBCS er:
- Vid lokal excisjon med underminering og lukking
- Terapeutisk mastopeksi (brystløft)
- Terapeutisk reduksjonsplastikk
- Erstatning av volumtap med lappeplastikk
Dersom tumor er liten, ligger et sted i brystet der volumtap tolereres godt og brystet er tilstrekkelig stort, vil teknikk 1 være en god og enkel løsning med eller uten flytting av areolakomplekset. Teknikk 2–4 krever at kirurg har spesiell onkoplastisk kompetanse og vanligvis gjøres dette som et samarbeid mellom bryst- og plastikkirurg. Teknikk 2–3 innebærer rearrangering av kjertelvevet for å lukke defekten etter tumoreksisjon enten med en lappe- eller en rotasjonsplastikk av kjertelvevet. Ved et brystløft fjernes kun tumorområdet og i varierende grad hud. Det gir en moderat til liten reduksjon av brystets volum, men endrer dets form. Ved en reduksjonsplastikk fjerner man en god del av brystes volum og gjør brystet mindre.
Teknikk 4, erstatning av volumtap, benyttes der tumor versus brystets størrelse gjør at det gjenværende brystet blir for lite eller at kjerteldefekten ikke kan lukkes med en intern plastikk. Man må da vurdere å tilføre nytt vev fra brystets omgivelse. Lapper basert på blodtilførsel fra intercostalarterienes perforatorer både medialt (MICAP), anteriørt (AICAP) og lateralt (LICAP) i forhold til brystkassen kan tilføre brystet volum. I tillegg kan det lages større eller mindre lapper basert på den laterale thoracale arterien og den thoracodorsale arterien (latissimus dorsi, LD, TDAP) fra mer lateralt eller dorsalt på brystkassen (Hamdi et al., 2008; McCulley et al., 2015; Rusby et al., 2008).
Radiologiske undersøkelser etter OBCS
Til tross for til dels store remodelleringer av brystkjertelvevet i forbindelse med OBCS, er det ikke vist å medføre noen flere uklare mammografifunn med behov for biopsi 6 måneder, 2 og 5 år postoperativt (Piper et al., 2016).
Boost-bestråling etter OBCS
Indikasjon for strålebehandling med boost er den samme som ved BCT. Bruk av boost ved stråleterapi er vist å redusere lokale tilbakefall etter BCT og i særlig grad hos pasienter <40 (50) år, men har ikke vist overlevelsesgevinst (Bartelink et al., 2015). OBCS kan vanskeliggjøre boost- bestråling pga usikker lokalisering av primær tumorseng. Remodellering av brystet kan gjøre det umulig å gjenfinne opprinnelig tumorområde dersom sårhulen ikke merkes med klips som er plassert like etter tumorreseksjonen og før den onkoplastiske rekonstruksjonen (Furet et al., 2014; Schaverien et al., 2013). Klips gir bedre definering av området som bør bestråles med boost. Det forutsettes også en grundig operasjonsbeskrivelse og et nært samarbeid mellom kirurg og onkolog. På denne måten sikres at adekvat område får tiltenkt boost og at vev utenfor målområdet spares for unødvendig strålebelastning da dette kan medføre et dårligere kosmetisk resultat med mer fibrose (Murphy et al., 2011).
Reseksjonskanter ved BCT (A. S. Coates et al., 2015; Moran et al., 2014)
- Ved BCT for invasivt carsinom skal det være frie reseksjonskanter både når det gjelder invasivt carsinom og DCIS (ink not on tumor). Det er ikke nødvendig med reseksjonsmarginer til / avstand mellom tumor og reseksjonsflate (uavhengig av om DCIS er i kontinuum med invasivt carcinom eller isolert fokus).
Det samme gjelder for BCT etter neoadjuvant behandling.
Dersom det er tvil om reseksjonskantene er frie/ evt påvist ikke frie kanter, må det gjøres reoperasjon i form av re-reseksjon eller mastektomi. Dersom det blir behov for flere re-reseksjoner, bør man overveie mastektomi, fordi det er holdepunkter for sammenheng mellom gjentatte reseksjoner og lokalt residiv i brystet (Menes et al., 2005).
- Ved BCT for kun DCIS «pure DCIS» skal det fortsatt være ≥2 mm reseksjonsmarginer (avstand mellom tumorvev og reseksjonskant) (kfr kapittel "Premaligne forandringer i brystet", avsnitt "Ductalt carcinoma in situ (DCIS)", samt kapittel "Oversikt over behandlings- og kontrollforslag ved premaligne tilstander") (Morrow et al., 2016). Årsak til dette er at disse pasientene ikke mottar adjuvant endokrin behandling eller cellegiftbehandling og at de i noen tilfeller (DCIS grad 1 ≤10mm) ikke mottar postoperativ strålebehandling.
Ablatio/mastektomi
Indikasjon
- Når brystbevarende kirurgi ikke er indisert ut fra ovennevnte kriterier
- Når pasienten ikke ønsker brystbevarende behandling, inkludert strålebehandling
- Når strålebehandling ikke lar seg gjennomføre.
- Ved lokalt tilbakefall/ny tumor etter tidligere brystbevarende kirurgi med postoperativ stråleterapi. (Det finnes dog ingen randomiserte studier på hvilken kirurgisk behandling som er best ved lokale tilbakefall.)
- Ved inflammatorisk cancer eller annen T4 cancer etter neoadjuvant behandling
- Genmutasjonsbærere (i henhold til kapittelet om arvelig brystkreft): Profylaktisk bilateral mastektomi med eller uten primær rekonstruksjon.
Typer mastektomi
- Enkel mastektomi med eller uten aksilleinngrep
- Hudbesparende mastektomi med fjerning av areolamamillekomplekset (SSM)
- Hudbesparende mastektomi med bevaring av areolamamillekomplekset (NSM)
For pasienter som ikke er genbærere er det ikke generell indikasjon for profylaktisk fjerning av kontralateralt bryst (med eller uten rekonstruksjon) ved diagnose brystkreft da dette ikke bedrer prognosen.
Teknikk
Enkel mastektomi
Kirurgisk snittføring bør forut for operasjonen tegnes opp på pasientene (spesielt de adipøse) i oppreist stilling. Dette fordi brystkjertelen i liggende stilling glir lateralt og oppad og det blir vanskelig å bedømme hvorledes arret vil fremtre i stående eller sittende stilling. Dette er sann-synligvis den hyppigste årsak til at det oppstår hudoverskudd i relasjon til arret lateralt og medialt. Hele brystkjertelen inkludert processus axillaris må fjernes komplett ned til pectoralisfascien. Eventuelt tidligere sårhuler må omfattes av inngrepet. Generelt sett bør den nederste incisjonen legges så langt caudalt som mulig og helst i inframammærfolden. Aksilleinngrep kan vanligvis gjøres gjennom samme snitt.
Oftest brukes båtformet snitt, og det bør legges slik at det etter lukking blir horisontalt og ikke på skrå inn i aksillen. Det tilstrebes velsirkulerte lapper med lik tykkelse uten at en etterlater kjertelvev. Lappene kan være fra mm til cm tykke. Det er ikke vist noen sikker korrelasjon mellom mastektomiplanets tykkelse, BMI, alder eller bryststørrelse (Robertson et al., 2014). Det vil i de fleste tilfeller være restkjertelvev og en bør være spesielt oppmerksom på ikke å etterlate vev i ytterkantene av brystet (Griepsma et al., 2014). Preparatet orienteres i enighet med patolog. Snittføringen må modifiseres dersom tumor er beliggende slik at det blir nødvendig. Dren er ikke nødvendig, men kan benyttes slik den enkelte avdeling finner det best. Ved bruk av dren bør dette dog ikke ligge for lenge på grunn av infeksjonsfare.
NB: Hel bakre reseksjonsflate er avgjørende for patologens vurdering. Ved muskelnær tumor litt av pectoralismuskulatur eksideres for å sikre radikalitet.
Hudbesparende mastektomi
Ved primær rekonstruksjon gjenvinnes brystets volum og form med et implantat (protese-rekonstruksjon) alternativt kroppens eget vev (autolog rekonstruksjon). Anbefaling om primær rekonstruksjon bør være tatt i et tverrfaglig møte med onkologisk kompetanse. Teknikken er en sikker metode uten kjent økt risiko for lokalt tilbakefall, selv om observasjons¬tiden i de fleste studier er kort og det ikke finnes i randomiserte prospektive studier der en sammen¬ligner primær rekonstruksjon med sekundær rekonstruksjon eller ingen rekonstruksjon. Valget mellom primær eller sekundær rekonstruksjon bestemmes av ulike pasient- og sykdomsmessige forhold se kapittel "Rekonstruktiv kirurgi etter mastektomi".
Ved planlagt primær rekonstruksjon gjøres mastektomien som et hudbesparende inngrep. Areola kan bevares etter individuelle vurderinger basert på tumors avstand til areola, DCIS utbredelse og tumorstørrelse (Timbrell et al., 2017). Det anbefales enten å ta separate biopsier retroareolært som merkes spesielt for patologisk undersøkelse eller at det settes en merketråd i det subareolære området. Peroperativt frysesnitt anbefales ikke. Snittføring tilpasses lokalisasjon av tumorområdet samt brystets form og størrelse. Det tilstrebes velsirku¬lerte lapper med lik tykkelse uten at en etterlater kjertelvev. Lappene kan være fra mm til cm tykke (se avsnittet over om konvensjonell brystbevarende operasjon (BCT)).
En studie har vist at risiko for lokalt recidiv etter mastektomi ved utbredt DCIS er større dersom det er gjort hudbesparende inngrep kontra konvensjonell mastektomi (Zhang et al., 2015). Risikoen synes størst hos unge pasienter og dersom det er knappe marginer ventralt. Det anbefales derfor at man hos disse tilstreber 2 mm margin ventralt.
Flytskjema for brystkirurgiske alternativ ved brystkreft og/eller DCIS
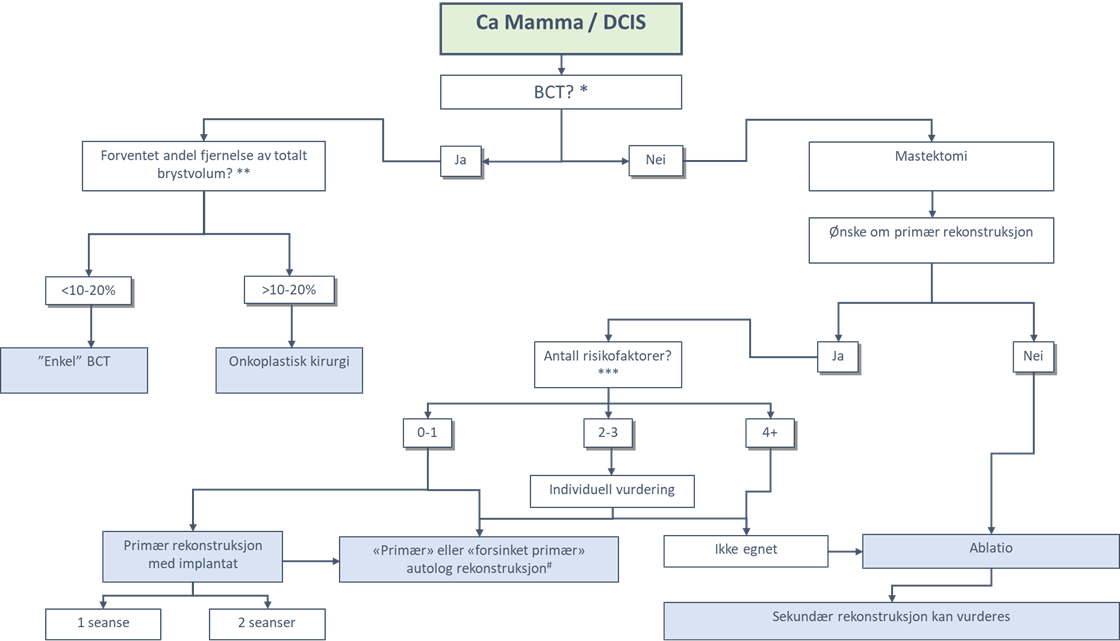
Vaktpostlymfeknutebiopsi (SNB) (evidensnivå A)
Indikasjoner
- Ved invasivt karsinom i stadium cT1-T3 uten påvist klinisk palpable lymfeknutemetastaser eller ≤ 2 ikke palpable axillære patologiske lymfeknuter verifisert ved ul og FNAC/grovnålsbiopsi
- Etter neoadjuvant systemisk behandling ved initialt cT1-3 tumorstørrelse og cN0-1 lymfeknutestatus hvor nodal status etter behandling er ycN0 vurdert palpatorisk og eventuelt med ultralyd eller MR
- Ved utbredt DCIS der det skal gjøres ablatio. Det skal imidlertid ikke gjøres AD i denne situasjonen dersom man ikke påviser SN.
- Ved brystbevarende kirurgi for DCIS er det ikke indisert med SNB. Skulle det i endelig diagnose vise seg å foreligge invasivt carsinom, kan SNB gjøres i etterkant.
Teknikk SNB
Vaktpostlymfeknuten er den/de lymfeknutene som drenerer svulsten i brystet. Vaktpostlymfeknutediagnostikken er utviklet i en rekke randomiserte studier som har vist lav falsk negativ rate (FNR), lav armmorbiditet og lokale tilbakefall i aksillen sammenlignet med aksilledisseksjon (Bartels et al., 2023; de Boniface et al., 2024; Giuliano et al., 2017). Vaktpostlymfeknuten identifiseres ved hjelp av en tracer (radioaktiv isotop, blåfarge, supramagnetisk jernoxid) og palpasjon,- eksideres og sendes deretter til histopatologisk undersøkelse (Giuliano et al., 1997; Krag et al., 2007; Krag et al., 2010; Kuehn et al., 2004; Mansel et al., 2006; Veronesi et al., 1999; Veronesi et al., 2010).
Antall SNB eksidert er relatert til skulder-arm morbiditet, som igjen har innvirkning på livskvalitet (Bartels et al., 2023). Omfanget av SNB diagnostikk bør ha lav FNR med minimal morbiditet. Det er ikke uvanlig at det er flere enn en vaktpostlymfeknute. Randomiserte studier har vist at antall eksiderte vaktpostlymfeknuter reduserer FNR ved primær kirurgi. NSABP-B 32 studien viste at FNR var< 10 % for ≥ 2 SN, men uten signifikant ytterligere reduksjon ved 3-5 (6,9 % for tre SN, 5,5 % for fire SN og 1 % for fem eller flere SN) (Biganzoli et al., 2017; Harlow et al., 2005; Krag et al., 2010). Ved neoadjuvant behandling er FNR vist å være høyere.
Flere tracere kan kombineres for å redusere FNR. Ved primær kirurgi og ved neoadjuvant behandling der det ikke er påvist metastaser ved diagnosetidspunktet (cN0) er en tracer tilstrekkelig for å oppnå tilfredstillende deteksjonsrate og lav FNR rate som er på omkring 6 -7% (Geng et al., 2016; Hunt et al., 2009; Tan et al., 2011).
En andel cN1 kan ved respons på neoadjuvant behandling konverteres til ycN0. FNR i denne situasjonene er vist å være økt til omkring 10% men kan reduseres ved TAD (targeted axillary dissection) (FNR 2-4%) dvs eksisjon av merket patologisk lymfeknute og sentinel node diagnostikk eller SNB dual tracer der man fjerner minst tre lymfeknter som inkluderer minst 1–2 blå eller radioaktive lymfeknuter hvor de/den resterende er palpabel/papable lymfeknuter (FNR 5-9%) (Boughey et al., 2013; Caudle et al., 2016; Kuehn et al., 2013; Kuemmel et al., 2022).
Frysesnittundersøkelse av SNB har høy sensitivitet for makrometastaser men anbefales ikke som rutine. Dette er resurskrevende og forbruker vevsmateriale men er ved neoadjuvant behandling nyttig for å unngå reoperasjoner i tilfeller der det er usikkerhet omkring gjenværende malignitet i aksillære lymfeknuter (Elshanbary et al., 2022). Komplett patologisk respons i aksillen oppnås i 45–60% ved trippelnegativ og HER2-positiv sykdom og 18–35% Luminal A og B sykdom (Samiei et al., 2021). Immunhistokjemisk undersøkelse av SN anbefales ikke som basisrutine, men anbefales dersom primærtumor er av lobulær type (Weaver et al., 2011). Utført på frysesnitt vil dette redusere FNR ved lobulært karsinom.
Lymfoscintigrafi er sjelden nødvendig. Dersom man likevel skulle ønske en visualisering av hvor (aksille eller parasternalt, ipsi- eller kontalateralt) og om det er opptak av radioaktivitet, kan dette gjøres etter injeksjon av radioaktivt isotop. Ved opptak parasternalt på scintigram, bør det gjøres aksilleeksplorasjon først. Det er fra litteraturen usikkert om det er indisert å eksidere eventuell vaktpostlymfeknute parasternalt, der den vesentligste gevinsten vil være i de meget få tilfeller hvor dette funnet vil føre til annen og mer adjuvant behandling, dersom vaktpostlymfeknuten i aksillen er negativ. Det er ingen holdepunkter for at fjerning av lymfeknuter parasternalt påvirker residivfrekvensen
Ved høy alder, høy BMI, stor tumor og utbredte metastaser til aksillen er det økt risiko for ikke å finne SNB (1-2%). Ved klinisk negativ aksille anbefales en begrenset aksilledisseksjon som et stadieinngrep der det eksideres minst 4 lymfeknuter selv om risikoen for metastaser til aksillære lymfeknuter i disse tilfellene er økt (Magnoni et al., 2022; Verheuvel et al., 2018).
Aksilledisseksjon etter SNB ved primær kirurgi
Det er indikasjon for SNB ved invasivt karsinom cT1-T3 uten påvist klinisk palpable lymfeknutemetastaser eller ≤ 2 ikke palpable aksillære patologiske lymfeknuter verifisert ved ul og FNAC/grovnålsbiopsi.
Det er ikke indikasjon for aksilledisseksjon ved negativ SNB eller ≤2 mm metastasefokus uavhengig av om det gjøres ablatio eller BCT (Cserni et al., 2004; Sola et al., 2013).
For SN positiv med metastasefokus > 2 mm kan AD utelates dersom alle følgende kriterier er oppfylt (Bartels et al., 2023; de Boniface et al., 2024; Giuliano et al., 2017; Savolt et al., 2017):
- 1 eller 2 positive SN
- Planlagt systemisk adjuvant behandling
- Planlagt ekstern stråleterapi mot lokoregionalt område
- Ikke preoperativ kjemoterapi
Ved SN svikt og cN0 status anbefales en begrenset aksilledisseksjon/aksillesampling som et stadieinngrep (minst 4 lymfeknuter).
Utelatelse av SNB ved primær kirurgi
Hos postmenopausale pasienter diagnostisert med cT1G1-2N0, HR+, HER2- NST tumores har ASCO guidelines (Park et al., 2025), med støtte fra tidligere rapporterte studier (Agresti et al., 2014; Gentilini et al., 2023; Liang et al., 2017; Martelli et al., 2012; Reimer et al., 2025; Rudenstam et al., 2006), åpnet for å kunne utelate sentinel node biopsi dersom det gjøres brystbevarende kirurgi med påfølgende stråleterapi og endokrin behandling tilbys.
For postmenopausale kvinner med lavrisiko sykdom (unifokal ER+/HER2- negativ cT1/N0/ ikke lobulære cancere ≤ 2 cm/grad 1-2 kan SN utelates i tilfeller der det planlegges for brystbevarende kirurgi etterfulgt av helbrystbestråling og endokrin behandling. Delbrystbestråling ble ikke benyttet i SOUND og INSEMA og resultatene fra disse studiene er derfor usikre for pasienter som er aktuelle for denne type bestråling (Borm et al., 2025). Beslutning om å ikke utføre SN bør besluttes i MDT og ikke medføre eskalert onkologisk behandling som endokrin behandling og helbrystbestråling.
Selv om det er observert flere aksilleresidiv uten aksillekirurgi er det meget lav frekvens av slike residiver og ingen forskjell i overlevelse (Liang et al., 2017). Dersom undersøkelsene av operasjonspreparatet konkluderer med høyrere genomisk risikoprofil kan sekundær SN diagnostikk være aktuelt.
Aksillekirurgi etter neoadjuvant systemisk behandling
cT2-3N0 – ycT2-3N0
SNB etter neoadjuvant systemisk behandling hos cN0 pasienter har i prospektive studier og metaanalyser vist deteksjonsrate og falsk negativ rate på 6-7% og tilbakefallsrate i aksille 1,5%. Dette er tilsvarende som for de som ikke får denne typen behandling. Dersom det påvises negativ aksille etter preoperativ behandling (ycN0) anbefales derfor SNB diagnostikk med tilsvarende teknikk som ved primærkirurgi. Ved SNB negativitet skal det ikke gjøres AD.
cT1-3N1 – ycT0-3N0
Isolert positiv intramammær lymfeknute, klassifiseres som cN1, men kan opereres med SNB som ved cN0.
En andel cN1 kan ved respons på neoadjuvant behandling konverteres til ycN0. Disse pasientene kan opereres med SNB uten forhøyet risiko for tilbakefall i aksillen og med mindre arm morbiditet. FNR er tilsvarende som ved primær kirurgi ved TAD (targeted axillary dissection) (2-4%) dvs eksisjon av merket patologisk lymfeknute og sentinel node diagnostikk eller SNB dual tracer der man fjerner minst tre lymfeknuter som inkluderer minst 1–2 blå eller radioaktive lymfeknuter hvor de/den resterende er palpabel/palpable lymfeknuter (5-9%). Frysesnitt baseres på responsevaluering og anbefales kun der det er usikkerhet om ycN status.
Det gjøres AD dersom SNB/TAD mislykkes.
Ved SN positivitet (> 0.2 mm) er det indikasjon for aksilledisseksjon. Hos disse pasientene finner en ytterligere metastaser hos >60 % (Moo et al., 2018).
cT1-3N2-3
Ved cT2-3N2-3 før neoadjuvant behandling skal det gjøres aksilledisseksjon uten SNB, uavhengig av tumor¬respons.
cT4N0-3
Pasienter med cT4N0 tumores er generelt ikke kandidater for SNB og anbefales aksilledisseksjon (AD). I enkelte tilfeller som for eksempel ved lokalisert ulcerasjon i hud (cT4b) og god respons på neoadjuvant behandling kan SNB vurderes (Park et al., 2025).
Utdypende kommentar spesielt knyttet til pasienter med cT2cN0 tumores:
Stadig flere pasienter i denne gruppen får neoadjuvant behandling. Dersom de etter neoadjuvant behandling har positiv SN (>0,2 mm) skal det gjennomføres AD, selv om det ved cT2 tumores uten neoadjuvant behandling ikke det er nødvendig i henhold til Z0011 studien. Årsaken er at responsen på den neoadjuvante behandlingen hos disse pasientene ikke oppfattes som god nok (fortsatt tilstedeværende mikrometastaser). Vanligvis skal pasienter med cT2cN0 stadium hvor endelig klassifisering av aksillen etter operasjonen er pN1(mi), heller ikke ha strålebehandling mot regionale lymfeknuter, i motsetning til pasienter med cT3/4 tumores.
Aksilledisseksjon (AD)
Indikasjon
- Som ledd i primærbehandlingen ved påviste lymfeknutemetastaser (preoperativt/peroperativt eller postoperativt) i henhold til retningslinjer beskrevet ovenfor.
- cT1-3N1 – ycT0-3N0, dersom ikke vaktpostlymfeknuter finnes ved operasjon etter neoadjuvant behandling.
Teknikk
Snitt enten som eget tverrsnitt i nedre del av aksille eller ved ablatio gjennom samme snitt. Alt aksillefett som inkluderer lymfeknuter i nivå 1 og 2 fjernes. Det vil si opp til vena axillaris, medialt ved mediale kant av m. pectoralis minor, bakre begrensning nervus thoracodorsalis/musculus latissimus dorsi. Nervus thoracodorsalis og nervus thoracicus longus må identifiseres og respekteres. Costobrachiale nerver bør identifiseres, om mulig bevares og beskrives i operasjonsbeskrivelsen. Ved brystbevarende kirurgi er det spesielt viktig å eksplorere godt i nedre, fremre del av aksillen slik at man ikke overser lymfeknuter der. Ublodig teknikk slik at man har god oversikt over strukturene peroperativt. Vær forsiktig med diatermibruk nær nervene.
Intramammær lymfeknutemetastase
Nye oversikter konkluderer med at det ikke er nødvendig med AD ut over hva det for øvrig er indikasjon for (på bakgrunn av SN og sykdomssituasjon for øvrig) (Diaz et al., 2012).
Utdypende kommentar om TAD (Targeted Axillary Dissection)
TAD er en prosedyre der vaktpostdiagnostikk og målrettet fjerning av en tidligere merket lymfeknute i aksillen kombineres. Lymfeknuten kan merkes med ulike metoder, f.eks. metallklips eller Savi Scout, og vaktpostprosedyren gjøres ellers på vanlig måte. Hensikten er å sikre at påviste metastase tas med ut uten å gjøre aksilledisseksjon. Målet er å evaluere respons på neoadjuvant behandling både i påvist lymfeknutemetastase og i SNB. I over halvparten av tilfellene er den markerte lymfeknuten også SNB. TAD kan være en strategi for å skreddersy aksillekirurgien, og metoden kan spare noen pasienter for aksilledisseksjon. Det er foreløpig usikre data på nytte av TAD ved primær kirurgisk behandling.