Når barn får kreft, får de plager på grunn av både sykdommen og behandlingen. Kanskje har de andre sykdommer i tillegg. Derfor er det er viktig å ivareta «hele» barnet for å bevare en god livskvalitet. Foreldre og barn trenger tilpasset og tilrettelagt informasjon om sykdom og bivirkninger. Informasjonen må tilpasses barnets alder og foreldre og barns kulturelle og språklige tilhørighet. Det er viktig å involvere støttepersonell som fastlege, sykepleier, fysioterapeut, dietetiker, tannpleier, sosionom, prest, skole og barnehage etter behov. De eldste barna vil ofte ha andre informasjonsbehov underveis, som for eksempel informasjon om seksualitet og kreft, og de kan ha behov for diskusjon rundt eksistensielle problemer.
Helsesøster bør involveres om familien ønsker det. Det er viktig med samtykke før eksterne involveres.
Symptomer som oppstår underveis, kan være uttrykk for mer eller mindre alvorlige sykdoms – eller behandlingsrelaterte komplikasjoner. Det dreier seg om anemi, infeksjoner og tumorlysesyndrom. I hvilken grad slike komplikasjoner oppstår, avspeiler intensiteten av cellegiftbehandlingen, kreftsykdommen, barnets tilstand på diagnosetidspunkt og genetiske forhold.
Støttebehandling omfatter symptomlindring med antiemetika, analgetika, steroider, H2‑reseptorantagonister, protonpumpehemmere, benzodiazepiner og laksantia. Det gis ofte antibiotika, blodprodukter, væske og elektrolytter, hematopoietiske vekstfaktorer og noen ganger antiepileptika og antikoagulantia. Barnets ernæringstilstand bør tidlig ivaretas, og bruk av nasogastrisk sonde, perkutan gastrostomi eller parenteral ernæring er vanlig.
Profylaktisk antimikrobiellbehandling
Behandling av barn med cellegift, stråleterapi og eventuell organtransplantasjon øker risikoen for infeksjoner. Spesielt behandling med langvarig myelosuppresjon med slimhinneaffeksjon, sentrale katetre og langvarig sykehusopphold, hvor barnet er utsatt for nosokomielle organismer, bidrar til å øke infeksjonsrisikoen. Det stilles derfor store krav til behandlende avdeling, som må ha rutiner for å redusere smittespredning og for opplæring av barn og familie i profylaktisk munnhygiene og alminnelige hygieniske prinsipper. Retningslinjer for infeksjonsprofylakse i forbindelse med kreftbehandling finnes ofte beskrevet i dagens protokoller som det henvises til på nopho.net og barnekreftportalen.no. De hyppigste agens som krever profylaktisk behandling er Pneumocystis jirovecii, sopp og Varizella zoster virus (VZV). Stamcelletransplantasjon er en spesiell situasjon med langvarig utslått immunforsvar. Barn i denne situasjonen kan utvikle kronisk GHVD og kan ha forlenget behov for profylaktisk behandling mot Pneumocystis jirovecii, sopp og virus (CMV, HSV og VZV). Indikasjon og dosering av antibiotika er beskrevet i Barnelegeforeningens generelle veileder og akuttveileder for pediatri (Akuttveileder i pediatri [e-bok], 2013; Generell veileder i pediatri [e-bok], 2012).
Retningslinjer for bruk av G-CSF
G-CSF brukes som primærprofylakse for å kunne øke doseintensiten av cellegiftbehandlingen. Dette er aktuelt ved for eksempel HR-nevroblastom, som sekundærprofylakse hos pasienter som tidligere har utviklet nøytropen feber, og hos kritisk syke barn med langvarig nøytropen feber etter cellegiftbehandling. G-CSF (filgrastim, Neupogen®) doseres for barn med 5 µg/kg/dag s.c (NB høyere dose i forkant av stamcellehøsting, vanligvis 10 µg/kg/dag). Varighet av behandlingen er inntil nøytrofile > 5 x 109/L en dag eller > 1 x 109/L i tre dager eller i henhold til protokoll.
Transfusjon
Anemi ved malign sykdom er ofte multifaktoriell. I de fleste tilfeller er kjemoterapien årsak, men også hemning av erytropoiesen, benmargsmetastasering, blødning og mangelfull ernæring spiller en rolle. Det er per i dag ingen konsensus om indikasjon for transfusjon av SAGMAN-erytrocyttkonsentrat i kreftbehandling, og beslutningen tas etter vurdering av barnets diagnose, allmenntilstand og forventede forløp. Den kliniske beslutningsterskel for transfusjon vil endres under behandlingsforløpet, hvor barnet tilvenner seg en lavere hemoglobinkonsentrasjon. På diagnosetidspunkt kan barnet ha svært lav hemoglobinkonsentrasjon (< 5 g/dL), og hyppige, mindre transfusjoner er aktuelt. I noen tilfeller, som ved nyoppdaget leukemi, kan det være en fordel med lav hemoglobinkonsentrasjon for å begrense viskositeten og risikoen for leukostase (se også avsnitt "Hyperleukocytose og leukostase" i kapittel Akutte onkologiske tilstander). En ofte brukt grense for blodtransfusjon er 8 g/dL, bortsett fra perioder med stråleterapi hvor en grense på 10 g/dL anbefales. Indikasjonsstillingen må imidlertid vurderes individuelt ut fra barnets kliniske tilstand og om man kan forvente snarlig spontan økning (retikulocytter). Dosering av SAGMAN-erytrocyttkonsentrat: (Ønsket hemoglobinkonsentrasjon (g/dL)– aktuell hemoglobinkonsentrasjon) x vekt x 3. Vanligvis blir dette 10–20 mL/kg kroppsvekt.
Før planlagt stamcelletransplantasjon skal alle blodprodukter bestråles fra ca. 1 måned før til ca. 12 måneder etter. Se Barnelegeforeningens generelle veileder og akuttveileder for pediatri (Akuttveileder i pediatri [e-bok], 2013; Generell veileder i pediatri [e-bok], 2012).
Indikasjon for trombocytt-transfusjon ved trombocytopeni og redusert produksjon er oppsummert i tabellen nedenfor.
Dosering er: Barn < 25 kg: 15 ml/kg kroppsvekt. Barn > 25 kg: 1–2 enheter. Trombocyttene gis over 20–40 minutter.
| < 10 x 109/L | < 20 x 109/L | 20–40 x 109/L | < 50 x 109/L |
| Som hovedregel gis alltid trc |
| DIC i induksjonsfasen med uttalt hyperleukocytose | Ved diagnostisk lumbalpunksjon for ALL anbefales > 50 |
Ved blødning og trombocytopeni skal det alltid gis trombocytter.
Det henvises for øvrig til Generell veileder for pediatri (Generell veileder i pediatri [e-bok], 2012) om indikasjon for leukocyttfiltrering og bestråling av blodprodukter generelt samt referanse (Gibson et al., 2004).
Smertebehandling
Barn med kreft har ofte smerter på diagnosetidspunkt, og det er viktig å gi optimal smertelindring, både for at barnet skal ha det best mulig og for at barnet skal bevare tilliten til behandler. I de fleste tilfeller avtar behovet raskt etter start av cellegiftbehandling. For både leukemi, solide svulster og CNS-svulster vil det være perioder hvor barnet trenger intensivering av smertebehandlingen. Det er alltid viktig å avklare smerteårsak, smerte utbredelse, type smerter (somatisk og/eller visceral nociseptiv- eller nevrogen smerte), gradere smerten og avklare grad av engstelse som vil kunne forsterke smerten. Tidlig introduksjon av smerteskala tilpasset barnets alder kan hjelpe barnet å gradere smertene og behandler å optimalisere behandlingen. Smertelindring i terminalfasen er en spesialistoppgave og igangsettes av behandlende onkologisk avdeling (se eget kapitel om palliativ behandling).
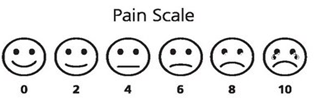
Vanlige prinsipper for smertebehandling kan brukes. Man starter med paracetamol som kan kombineres med NSAIDs (ibuprofen), og rask opptrapping med opiater. Forsiktighet med NSAIDs dersom barnet har redusert eller truende nyrefunksjon, får nefrotoksiske medikamenter/cellegift, ved moderat til alvorlig trombocytopeni og ved kjent allergi. For å finne barnets døgnbehov startes opiatbehandling med hurtigvirkende preparater, eventuelt med intravenøs tilførsel ved alvorlige smerter eller ved problemer med tablettinntak. Døgndosen kan senere gis som langtidsvirkende preparat, men det må alltid være mulighet for hurtigvirkende opiater ved gjennombruddssmerter og rask oppjustering av doser ved manglende effekt. Ved intensiv smertebehandling økes risikoen for obstipasjon, og bruk av laxantia anbefales. De fleste barn vil være innlagt i slike situasjoner, og behandlingen styres av smerteteam. For supplerende informasjon henvises det til: childcancerpain.org, legemiddelhandboka.no og generell veileder i Pediatri.
Ikke-medikamentell smertelindring bør vektlegges: En barnepsykiater og psykolog skal i dag ha kompetanse på en rekke ikke-medikamentelle symptomlindrende teknikker; bl.a. ift smerte og kvalme. Spesielt gjelder dette ved tillegg av angst og uro (som nesten alltid vil være til stede). Eksempler på psykologiske intervensjoner som ledd i smertelindring er; avledning, narrativer, avspenning og pusteteknikker, eksternaliseringsteknikker, hypnoterapi, korttidsterapi (CBT) m.m. Et viktig ledd i smertelindring av barn, er god ivaretagelse/trygging av foreldre/pårørende.