Fagbegrep i delkapitlet:
- Aftøs stomatitt Tilstand med flere små, runde og hvite ømfintlige sår på munnslimhinnen.
- Candidose Gjærsoppinfeksjon som manifesterer seg som et grå-hvitt belegg på slimhinnene, og forekommer i noen tilfeller ved antibiotikabehandling.
- Cystisk fibrose Medfødt arvelig lidelse som manifesterer som seigt og tykt slim som blokkerer luftveiene.
- Edentulisme Fullstendig mangel på tenner på grunn av sykdom eller uttrekking.
- Ehlers-Danlos’ syndrom En heterogen gruppe av genetisk drevne tilstander som alle karakteriseres ved økt elastisitet av huden, og at leddene kan beveges utover det normale.
- Karies En tilstand hvor tennene blir skadet som følge av syre fra bakterier og fører til tap av mineraler i emaljen. Skaden som oppstår kalles ofte hull i tennene eller tannråte.
- Lichen planus Hudsykdom som også kan oppstå som et hvitt, nettaktig utslett i munnslimhinnen.
- Metabolsk syndrom Samlebetegnelse på risikofaktorer for hjerte- og karsykdom og diabetes type 2, typisk karakterisert ved abdominal fedme og arvelige egenskaper.
- Mineraliseringsforstyrrelser i emaljen Hvite eller brune dårlig mineraliserte områder på tennene(kvalitativ defekt), kan gi sterk ising i tennene i alvorligere tilfeller. Andre forstyrrelser kan være hypoplastisk emalje (kvantitativ defekt).
- Munntørrhet Tilstand med for lite spyttutskillelse. Litteraturen skiller mellom subjektivt opplevd munntørrhet (xerostomi) og målt munntørrhet (hyposalivasjon).
- Periodontitt Betennelse av vevet rundt tannen (periodontiet). Ødelegger tannens festefibre og det omgivende kjevebeinet helt eller delvis.
- Periimplantitt Infeksjoner rundt tannimplantater. I motsetning til periodontitt som rammer vevet rundt tannen er disse infeksjonene i selve beinet implantatet er festet til og er vanskeligere å behandle enn periodontitt.
- Retts syndrom Svært sjelden arvelig sykdom
- Sialoré Ekstrem mengde spytt som manifestasjon på underliggende sykdom.
- Sjøgrens syndrom Autoimmun bindevevssykdom, karakterisert ved vedvarende tørrhet, særlig i øyne og munn.
- Stomatitt Samlebetegnelse på munnslimhinnebetennelse.
- Talassemi Er en arvelig blodsykdom som rammer hemoglobinet i de røde blodcelle og gir anemi.
I dette delkapitlet tar vi for oss de systematiske oversiktene og beskrivelsene i forvaltningskildene hvor ulike somatiske tilstander eksponerer ulike grupper for orale tilstander. Det er selvsagt diskuterbart om samtlige av disse utfallene er faktiske orale manifestasjoner på de studerte somatiske tilstandene, eller om de er selvstendige tilstander som oppstår som følge av en prosess igangsatt av de somatiske tilstandene.
I Figur 3-4 viser vi hvilke somatiske tilstander (venstre kolonne) som antatt eksponerer for orale manifestasjoner (høyre kolonne). Tykkere koblinger viser mer frekvente sammenhenger i utvalget enn tynne. I det følgende beskriver vi oversiktenes sammenhenger med rekkefølge basert på frekvens i utvalget fra flest til færrest.
Figur 3-4 Orale manifestasjoner på somatisk sykdom beskrevet i systematiske oversikter
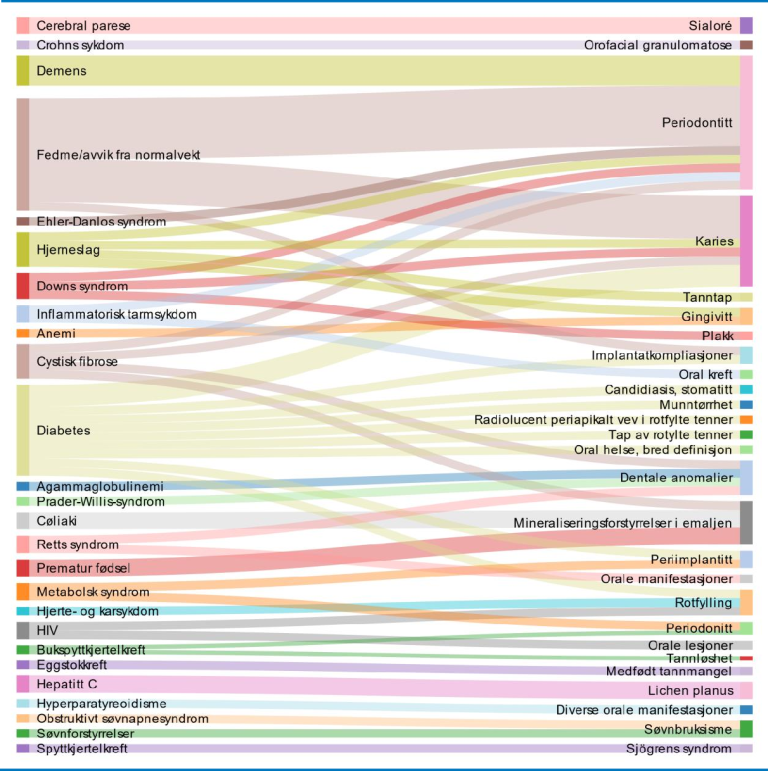
3.2.1 Fedme eller avvik fra normalvekt
I litteratursøket identifiserte vi 16 studier [10-25] som undersøkte assosiasjoner mellom undervekt, overvekt eller fedme, og orale tilstander. I 14 av disse var fedme (kroppsmasseindeks (KMI) ≥ 30) eksponeringsfaktoren, mens én inkluderte også overvektige (KMI ≥ 25) [24], og én inkluderte både undervektige (KMI < 18,5) og overvektige i tillegg til personer med fedme [21].
Fedme og karies
Seks av oppsummeringene i vårt utvalg undersøkte sammenhengen mellom fedme og karies. Fem fokuserte på denne assosiasjonen for barn og unge [10, 18, 19, 21, 25], og i én var populasjonen voksne [20].
Chen m.fl. (2018) undersøkte assosiasjonen mellom forekomsten av karies og samtlige KMI- grupper hos barn basert på 14 studier med totalt 44 000 inkluderte personer. KMI- gruppetilhørighet var ikke en signifikant forklaringsvariabel av kariesforekomst, men det ble funnet signifikante forskjeller i forekomsten da de grupperte primærstudiene etter inntektsnivået i landet hvor studien ble gjort. De fant at barn med fedme i høyinntektsland hadde signifikant høyere forekomst av karies enn barn med fedme i lavinntektsland. Forfatternes forklaring på denne ulikheten var at en assosiasjon mellom fedme og karies trolig går via dietten, og at barn i høyinntektsland trolig har høyere tilgang på godteri enn barn i lavinntektsland [10]. Dette kan derfor gi både fedme og karies i høyinntektsland, slik at diett trolig er en konfunderende variabel i denne assosiasjonen.
En eldre oppsummering av Hayden m.fl. (2013) undersøkte også assosiasjonen mellom fedme og karies hos barn i tradisjonelt industrialiserte land og ny-industrialiserte land. De fant at barn med fedme i land som lenge har vært industrialisert hadde signifikant høyere kariesforekomst enn barn med fedme i nylig industrialiserte land [19]. Også her er det sannsynlig at diett spiller en viktig rolle i assosiasjonen.
De tre øvrige oppsummeringene som undersøkte assosiasjonen mellom fedme og karies hos barn kom til motstridende og inkonsekvente konklusjoner. Kantovitz m.fl. (2006) inkluderte studier hvor resultatet talte både for og imot at fedme er assosiert med karies hos barn [25].
Hooley m.fl. (2012) fant derimot at både undervektige og overvektige barn hadde høyere kariesforekomst enn normalvektige [21]. De diskuterte at begge grupper kan ha høyere sannsynlighet for å ha lavere sosioøkonomisk status, og at dette er en mulig såkalt mediator for sammenhengen. Mediatorer er variabler som korrelerer med både eksponerings- og utfallsvariablene, og ligger mellom disse i årsakskjeden. Paisi m.fl. (2019) konkluderte med at det kan være en sammenheng mellom fedme og karies hos barn i skolealder, men også at dette ikke virket å være tilfelle hos yngre barn [18].
Til forskjell fra de fem andre oversiktene som undersøkte assosiasjonen mellom fedme og karies, inkluderte Silva m.fl. (2013) kun nyere studier (2005-2012). Denne avgrensningen ble gjort for å reflektere sammenhengen gitt et moderne kosthold, og fordi det i mange land i senere tid er blitt tilsatt fluor i vannforsyningen.
Oppsummeringen fant ikke tilstrekkelig evidens for å støtte en sammenheng mellom fedme og karies hos voksne [20].
Fedme og periodontitt
Vi identifiserte åtte systematiske oppsummeringer som undersøkte sammenhengen mellom fedme eller overvekt og periodontitt [12, 15-17]. Samtlige av oppsummeringene konkluderte at det var en signifikant sammenheng mellom fedme og periodontitt.
Selv om de ikke var av de nyeste oppsummeringene, hadde publikasjonene av Keller m.fl. (2015) og Nascimento m.fl. (2015) best datagrunnlag. Keller m.fl. (2015) inkluderte 13 primærstudier hvorav åtte var prospektive longitudinelle studier med oppfølgingstid over 20 år. Dette studiedesignet reduserer risikoen for reversert kausalitet og konfundering fra kronisk sykdom ved innrulleringstidspunktet. Forfatterne konkluderte med at det var klare indikasjoner på at utvikling av overvekt, fedme, eller vektøkning generelt kan øke risikoen for utvikling av periodontitt, eller forverring av allerede manifestert periodontitt [17].
Nascimento m.fl. (2015) benyttet flere av de samme longitudinelle studiene som Keller m.fl. (2015) i sin metaanalyse. De beregnet at personer som gikk fra normalvektig til overvektig hadde 13 prosent høyere risiko for å utvikle periodontitt enn personer som forble normalvektige i samme periode. Samtidig hadde personer som utviklet fedme 30 prosent høyere risiko for periodontitt [15].
Akram m.fl. (2016) undersøkte spesifikt hvorvidt personer med periodontitt og fedme hadde en annen cytokinprofil i gingval væske enn normalvektige med periodontitt. De fant at personer med fedme i tillegg til periodontitten hadde signifikant høyere markører av enkelte inflammasjonsfremmende cytokiner enn normalvektige. Dette ble vurdert som en mulig driver for periodontittforekomsten [13].
Khan m.fl. (2018) så på sammenhengen mellom fedme og periodontitt hos barn mellom 13 og 17 år og unge voksne mellom 18 og 34 år. 17 av de 25 studiene inkludert i denne oppsummeringen fant en signifikant assosiasjon, og de aller fleste kontrollerte for inntak av sukkerholdig mat og brus, sosioøkonomisk status, og generell tannhygiene. Forfatterne drøftet ulike kliniske forklaringsmodeller for assosiasjonen. Én mulig forklaring, som også var tema i Akram m.fl. (2016), er at fettvev utsondrer cytokiner som TNF-α, som er assosiert med inflammasjon av periodontium, hvilket kan skade alveolarbeinet og brusken i periodontalt vev [12].
Sammenhengen mellom fedme og periodontitt ble i vårt utvalg først oppsummert av Chaffee og Weston (2010) og senere også av Suvan m.fl. (2011) og Moura-Grec m.fl. (2014). Felles for disse oppsummeringene er at de ble gjennomført omtrent på samme tid, inkluderte 19-31 studier og kom til nokså like konklusjoner; fedme kan øke risikoen for periodontitt med om lag 30-80 prosent sammenlignet med normalvektige [22-24].
Martens m.fl. (2017) fokuserte på forekomsten av periodontitt hos barn med fedme relativt til normalvektige barn i sin metaanalyse. Basert på sju primærstudier beregnet de at barn med fedme har omtrent 50 prosent høyere risiko for periodontitt enn normalvektige [16].
Fedme og tanntap, edentulisme og tannimplantatkomplikasjoner
I vårt utvalg av systematiske oppsummeringer med fedme som eksponeringsfaktor for orale utfall, var det kun to som vurderte andre utfall enn karies og periodontitt.
Nascimento m.fl. (2016) undersøkte hvorvidt fedme hos voksne kan føre til tap av tenner, delvis eller fullstendig edentulisme, eller reversert; om tanntap kan føre til fedme. De gjennomførte en metaanalyse basert på 16 primærstudier, med over 41 000 pasienter, som vekslet på eksponering- og utfallsfaktorene. De fleste av studiene var tverrsnittstudier hvor tanntap var eksponeringsfaktor for fedme. Forfatterne forankret denne påvirkningsretningen i hypotesen om at delvis eller fullstendig tannmangel kan vri en persons diett over fra å bestå av vektregulerende matvarer, som grønnsaker og fullkornsprodukter, over til matvarer som er lettere å innta, men som kan være mer kaloritette. Logikken bak påvirkningsretningen med fedme som eksponering var forankret i at fedme kan medføre karies og periodontitt, som til slutt leder til tap av tenner. Metaanalysen indikerte at begge retninger gav signifikant risikoøkning for utfallene, og det ble konkludert med at det trolig er et bidireksjonalt forhold mellom fedme og tanntap [14]. Tverrsnittstudier er ikke egnet til å avgjøre kausalitet, og denne oppsummeringen kunne derfor i strengeste mening ikke fastslå hvorvidt det faktisk er noe annet enn et bidireksjonalt forhold.
Monteiro m.fl. (2019) undersøkte litteraturen for å finne ut hvorvidt personer med fedme eller overvekt har flere komplikasjoner ved innsettelse av tannimplantater enn normalvektige. De fant ikke indikasjoner på at personer med fedme og overvekt er uegnet for tannimplantater, selv om at de kan ha forhøyde inflammasjonsmarkører rundt implantatet [11].
3.2.2 Diabetes
Litteratursøket identifiserte 16 systematiske oppsummeringer hvor diabetes eksponerte den undersøkte populasjonen for ulike orale tilstander [5, 26-38].
Diabetes og periodontitt
Fire av oversiktene med diabetes som eksponeringsfaktor omhandlet periodontitt som utfall. To av disse, de to nyeste, ble derimot vurdert til å ha større vitenskapelige mangler, og drøftes ikke videre [26, 28]. I avsnitt 3.3.1 diskuteres også denne sammenhengen ut ifra en antatt reversert påvirkningsretning.
Nascimento m.fl. (2018) inkluderte seks prospektive longitudinelle studier i sin metaanalyse, med målsetning om å kartlegge hvorvidt dårlig kontrollert diabetes er assosiert med utvikling eller forverring av periodontitt. De estimerte at personer som hadde dårlig kontrollert diabetes hadde 86 prosent høyere risiko for å utvikle, eller progrediere til verre, periodontitt enn personer uten diabetes eller godt kontrollert diabetes [27]. Forfatterne forankret sammenhengen i en hypotese om at personer med dårlig kontrollert diabetes vil ha forhøyet sirkulasjon av hvite blodceller og proinflammatoriske markører som over tid kan bryte ned vevet som omgir tennene.
Ismail m.fl. (2015) hadde som målsetning å oppsummere litteraturen for å beskrive den orale helsestatusen til barn med diabetes type 1, og vurdere hvorvidt de har dårligere periodontal helse enn barn uten diabetes 1. Oppsummeringen fant sprikende resultater for oral helsestatus hos barn med diabetes 1. Det var stor ulikhet i hva studiene oppgav av mål for periodontal status, samt stor variasjon i hvordan dette ble presentert i studiene. For disse barnas relative periodontal helse viste de inkluderte tverrsnittstudiene at barn med diabetes 1 hadde høyere gjennomsnittlig plakkindeks enn friske. Ingen av de inkluderte langtidsstudiene fant imidlertid noen signifikant forskjell. Oppsummert mente forfatterne at gjennomgangen tyder på at barn med diabetes 1 har generelt dårligere oral helse enn friske, men at det er usikkert hvorvidt de har dårligere periodontal helse [29].
Sammenhengen mellom diabetes og periodontitt ble diskutert i forvaltningskildene for samtlige av landene. Sundhedsstyrelsen i Danmark anbefaler med forutsetning om en sammenheng at personer med diabetes kan vurderes for hyppigere kontroll hos tannlegen [39]. I England anbefaler NICE at pasienter med diabetes bør tilstrebe å opprettholde god metabolsk kontroll for unngå at periodontitt utvikler seg [40].
Diabetes og karies
I utvalget fra litteraturoppsummeringen var det tre oversikter som fokuserte på sammenhengen mellom diabetes og karies.
Coelho m.fl. (2020) undersøkte om diabetikere har høyere prevalens av karies enn ikke-diabetikere, om diabetikere med dårlig metabolsk kontroll har høyere kariesforekomst enn de med god metabolsk kontroll, og hvorvidt diabetikere med langvarig sykdom har høyere kariesforekomst enn de med kortvarig sykdom. De inkluderte studier som omfattet både personer med diabetes type 1 og type 2 fra 69 primærstudier.
Resultatene ble sammenstilt i en metaanalyse. Diabetikere med type 1 hadde i gjennomsnitt signifikant høyere kariesprevalens enn friske kontrollpersoner, mens personer med diabetes type 2 hadde statistisk sett samme kariesforekomst som de friske kontrollpersonene. Kariesforekomsten var ikke signifikant ulik for personer med god eller dårlig metabolsk kontroll. Personer med langvarig diabetes type 1 hadde signifikant høyere forekomst av karies enn personer med kortvarig diabetes type 1. Det ble ikke funnet noen forskjell i forekomst gitt ulik varighet av diabetes type 2 [31].
I tillegg til at forfatterne studerte den periodontale helsen til barn med diabetes type 1, utforsket Ismail m.fl. (2015) hvorvidt forekomsten av karies var ulik for barn med og uten diabetes type 1. De avdekket motstridende funn: åtte studier fant at barn med diabetes type 1 hadde høyere kariesforekomst enn friske, og ni studier fant ingen statistisk signifikant forskjell. Forfatterne diskuterte hvorvidt disse sprikende resultatene kunne tilskrives ulikhet i metabolsk kontroll for barna i studiene. Dette forankret de i at den rådende oppfatningen av metabolsk kontroll for diabetes type 1 kan forklare kariesforekomst, som konkludert senere av Coelho m.fl. (2020). En annen forklaring på at det ikke ble funnet signifikant forskjell fra den generelle befolkningen var at flere i utvalget ble innrullert i forbindelse med at de oppsøkte tannlegebehandling. Dette kunne ha medført at kontrollgruppene var skjevt selektert og hadde høyere kariesforekomst enn den faktiske generelle befolkningen [29].
Denne sammenhengen ble drøftet sammen med periodontitt i forvaltningskildene med samme anbefalinger om hyppigere undersøkelser og opprettholdelse av god metabolsk kontroll.
Diabetes og tilstander i rotfylte tenner
To oppsummeringer fokuserte på orale utfall i rotfylte tenner for personer med diabetes. I studien av Segura-Egea m.fl. (2016), ville forfatterne finne ut hvorvidt diabetes kan påvirke utfallet av rotkanalbehandling. De gjennomførte en metaanalyse av resultatene fra sju primærstudier og fant at personer med diabetes hadde 42 prosent høyere forekomst av rotfylte tenner med denne typen vev rundt roten. Forfatterne konkluderte derfor med at diabetes kan være en viktig prognostisk faktor for utfallet av rotfylling [32].
Cabanillas-Balsera m.fl. (2019) undersøkte også diabetes som prognostisk faktor for rotkanalbehandling, mer spesifikt om personer med diabetes oftere må trekke rotfylte tenner enn personer uten diabetes. Også her ble det funnet at diabetes til en viss grad kan predikere dette, da personer med diabetes hadde over 140 prosent høyere risiko for at de rotfylte tennene etter hvert måtte trekkes enn personer uten diabetes [33].
Diabetes og tilstander i implantater
To av oppsummeringene i vårt utvalg undersøkte hvorvidt diabetes er assosiert med uheldige orale utfall for personer med tannimplantater [34, 35].
Monje m.fl. (2017) fant at personer med diabetes hadde omtrent 50 prosent signifikant høyere risiko for å utvikle periimplantitt enn personer uten diabetes [35]. Røyking er en kjent risikofaktor for blant annet implantatsvikt og kan gi dårligere resultat av implantatinnsetting. Oppsummeringen gjorde en tilleggsanalyse av artiklene hvor de sammenslo resultatene fra tre studier hvor røykere var ekskludert i både diabetesgruppen og kontrollgruppen.
Sammenlignet med ikke-røykere uten diabetes fant de at diabetes gav en relativ risiko for periimplantitt på 3,39 eller omtrent 240 % høyere risiko. Dette var kun basert på tre studier, og individuelt hadde ingen av studiene en signifikant høyere risiko for personer med diabetes. Den sammenstilte relative risiko var så vidt signifikant med svært bredt konfidensintervall.
Chrcanovic m.fl. (2014) undersøkte hvorvidt personer med diabetes har høyere forekomst av implantatsvikt enn ikke-diabetikere. De inkluderte 14 primærstudier som inkluderte om lag 6 000 personer i sin metaanalyse. Forfatterne konkluderte at diabetes ikke hadde noen innvirkning på forekomsten av implantatsvikt [34].
Diabetes og candidose, lichen planus, munntørrhet og stomatitt
Vårt utvalg inkluderte også mindre forekommende orale tilstander assosiert med diabetes.
Martorano-Fernandes m.fl. (2020) hadde som målsetning å oppsummere og sammenstille evidensen på prevalens av orale candidoseinfeksjoner og stomatitt blant diabetikere relativt til ikke-diabetikere. Publikasjonen forklarte at tidligere oppsummeringer på samme tema hadde tvilsom vitenskapelig kvalitet, og forfatterne satte seg som mål å gjenta øvelsen.
Metaanalysen av sju inkluderte studier fant ingen signifikant sammenheng mellom diabetes og candidose. Diabetes ble funnet å øke risikoen for stomatitt med 90 prosent, men dette må tolkes forsiktig da kvaliteten på primærstudiene var noe usikre [38].
Otero Rey m.fl. (2019) undersøkte forholdet mellom diabetes og oral lichen planus basert på et litteratursøk som inkluderte om lag 9 000 personer fra 22 studier. En metaanalyse fra ti av studiene ble gjennomført for å redegjøre for om diabetikere har høyere risiko for lichen planus enn ikke-diabetikere.
Prevalensen av lichen planus blant pasienter med diabetes varierte mellom 0,5 - 6,1 prosent i studiene, og metaanalysen viste at risikoen for lichen planus var omtrent 40 prosent høyere for diabetikere enn ikke- diabetikere [37].
Oppsummeringen til López-Pintor m.fl. (2016) undersøkte hvorvidt pasienter med diabetes har høyere forekomst av både subjektiv opplevelse av munntørrhet (xerostomi) og objektiv munntørrhet (hyposalivasjon), og om spyttsekresjonen er dårligere hos diabetespasienter enn friske kontrollpersoner. De identifiserte totalt 15 publikasjoner. For xerostomi ble det funnet at pasienter med diabetes hadde høyere prevalens (12 – 53 prosent) enn friske (0-30 prosent), men dette ble ikke funnet å være statistisk signifikant høyere enn hos kontrollgruppene. Kun én studie fant signifikant høyere forekomst av objektivt målt munntørrhet, men hadde en lavere terskelverdi for å gi et positivt testresultat enn hva som normalt brukes i klinikkene.
Det var derfor usikkerhet rundt hvorvidt dette var faktiske positive. Det var også stor variasjon i diagnostiske kriterier for målingene av spyttsekresjon. Forfatterne sammenfattet oppsummeringen med heterogenitet i målemetoder og ulikhet i graden av diabetes inkludert ikke gjorde det mulig å konkludere hvorvidt det er forskjell i munntørrhet for pasienter med diabetes og friske kontrollpersoner [36].
Tidligere paraplyoversikter over orale utfall assosiert til diabetes
Den siste oppsummeringen vi identifiserte med diabetes som eksponeringsfaktor for orale utfall, var en paraplyoversikt av systematiske oversikter utarbeidet for NHS i England [5]. Denne artikkelen bygger på nokså lik forutsetning som vår litteraturoppsummering. Datainnhentingen ble avgrenset til tiåret 2005-2015. I korte trekk ble det demonstrert at det finnes en mengde orale utfall assosiert med diabetes, herunder periodontitt, risiko for oral kreft, og tannimplantatsvikt. Med unntak av oral kreft som, vi ikke identifiserte, var funnene og flere av de inkluderte systematiske oversiktene generelt overlappende med våre funn for orale utfall assosiert med diabetes.
3.2.3 Metabolsk syndrom
Metabolsk syndrom er knyttet til både fedme og diabetes, og ble undersøkt som eksponeringsfaktor for orale tilstander i fire systematiske oversikter i vårt utvalg [41-44]. Felles for disse oversiktene er at samtlige påpeker at metabolsk syndrom trolig er knyttet til orale utfall, men at mangelen på longitudinelle studier gjør at det er vanskelig å være sikker på hva som driver assosiasjonene.
Metabolsk syndrom og periodontitt
Daudt m.fl. (2018) tok for seg sammenhengen mellom metabolsk syndrom og periodontitt fra studier publisert mellom 2006 og 2018 for å vurdere en mulig assosiasjon. De inkluderte 26 primærstudier som til sammen utgjorde observasjoner for over 52 000 personer. I sammenstillingen fant de at personer med metabolsk syndrom har omtrent 40 prosent høyere sannsynlighet for periodontitt enn friske kontrollpersoner [42].
En tidligere metaanalyse av Nibali m.fl. (2013) tilnærmet seg sammenhengen med åpning for at både metabolsk syndrom og periodontitt kunne være eksponerings- og utfallsfaktorer. De estimerte en signifikant assosiasjon mellom metabolsk syndrom og periodontitt, men gitt primærstudiene var konklusjonen om hvilken retning påvirkningen går ikke mulig å konstatere [41].
Metabolsk syndrom og tanntap
Souza m.fl. (2019) gjorde en nokså lik analyse som de to foregående og sammenstilte funn fra ni tverrsnittstudier ved hjelp av metaanalyse. Oversikten konkluderte at personer med påvist metabolsk syndrom hadde i gjennomsnitt tre færre tenner enn kontrollpersonene, og om lag 140 prosent høyere risiko for å ha et manglende funksjonelt tannsett [44].
Metabolsk syndrom og periimplantitt
Som beskrevet over har både fedme og diabetes vært undersøkt i forbindelse med periimplantitt. I og med at metabolsk syndrom kan øke risiko for disse somatiske tilstandene undersøkte Papi m.fl. (2018) en mulig kobling til periimplantitt. De gikk gjennom seks studier, men fant ingen tilstrekkelig indikasjon på at metabolsk syndrom og periimplantitt er assosiert.
3.2.4 Downs syndrom og annen psykisk utviklingshemming
Fire oversikter i vårt utvalg så på orale helseutfall for personer med Downs syndrom [45-48].
Downs syndrom, psykisk utviklingshemming og periodontitt
Den nyeste oppsummeringen på sammenhengen mellom Downs syndrom og periodontitt, Scalioni m.fl. (2018), søkte etter relevant litteratur i fem databaser fra første mulige dato frem til 2017. De inkluderte 23 studier i en kvalitativ gjennomgang, og sammenstilte resultatene fra tre av de med metaanalyse [45].
Metaanalysen sammenstilte indeksmål på periodontal helse, men viste ingen statistisk forskjell fra personer uten Downs syndrom.
I en eldre oversikt av Anders og Davis (2010) ble sammenhengen mellom Downs syndrom, psykisk utviklingshemming, og autisme vurdert som eksponeringsfaktorer for nedsatt oral helsestatus, herunder periodontitt. Denne oversikten inkluderte 27 primærstudier og presenterte ingen risikoestimater, men trakk konklusjonen at personer med psykisk utviklingshemming har høyere prevalens og alvorligere grad av periodontitt enn den generelle befolkning [46]. Downs syndrom ble trukket frem som en gruppe som hadde særlig risiko for periodontitt.
I England har Royal College of Surgeons publisert at barn med Downs syndrom har dårligere periodontal helse, selv med god oral hygiene [49].
I Norge har Regionsenter for habiliteringstjenesten for barn og unge ved Oslo Universitetssykehus skrevet at både barn og voksne med Downs syndrom har betydelig økt risiko for periodontal sykdom, som ofte kan føre til løsning av tenner for disse personene. Det forklares at endret bakterieflora i munnen, nedsatt immunforsvar og dårlig tannhygiene er trolig årsaker til dette [50].
Downs syndrom og karies
Til tross for at det i tilfeller kan synes å være en assosiasjon mellom Downs syndrom og periodontitt, fant vi få vitenskapelige studier som omtalte denne sammenhengen, herunder at personer med Downs syndrom var mer eksponert for karies enn den generelle befolkningen.
Moreira m.fl. (2016) undersøkte nullhypotesen om at personer med Downs syndrom har lik kariesforekomst som personer fra den generelle befolkning. De inkluderte 13 studier som inkluderte om lag 11 000 personer, men fant ikke noe vitenskapelig hold for å forkaste hypotesen om lik kariesforekomst hos personer med Downs syndrom og i generelle befolkningen [48].
Den ett år eldre metaanalysen til Deps m.fl. (2015) fant derimot at personer med Downs syndrom hadde signifikant 64 prosent lavere forekomst av karies enn i de inkluderte kontrollgruppene. Forfatterne påpekte imidlertid at resultatene burde tolkes forsiktig, gitt mangel på kontroll av relevante konfunderende variabler [47].
3.2.5 Inflammatorisk tarmsykdom
Vi identifiserte fire oversikter på assosiasjonen mellom inflammatorisk tarmsykdom og orale utfall, men tre av disse hadde mangelfull vitenskapelig kvalitet.
Den eneste studien med høy kvalitet var gjennomført av Papageorgiou m.fl. (2017). De ønsket å finne ut hvorvidt personer med inflammatorisk tarmsykdom har lik eller ulik prevalens av periodontal sykdom sammenlignet med personer uten inflammatorisk tarmsykdom. Det ble foretatt litteratursøk i ti databaser, med ni primærstudier som resultat.
Forekomsten av periodontitt ble sammenstilt som forskjell i gjennomsnitt per 1 000 personer mellom gruppene med og uten inflammatorisk tarmsykdom. Resultatet var en signifikant høyere forekomst, 330 flere per 1 000, hos personene med inflammatorisk tarmsykdom [51]. Også denne oppsummeringen påpekte at det manglet tilstrekkelige gode longitudinelle studier på sammenhengen til at kausaliteten kan sies å være kartlagt.
3.2.6 Cøliaki
Vi identifiserte to oppsummeringer av høy kvalitet som så på sammenhengen mellom cøliaki og mineraliseringsforstyrrelser i emaljen, og aftøs stomatitt [52, 53].
Mineraliseringsforstyrrelser er i hovedsak enten «molar incisor hypomineralisation» som først opptrer i jekslene, eller dental flurose som ofte skyldes fluorider i drikkevann [54].
Cøliaki har vært drøftet som mulig driver av mineraliseringsforstyrrelser, og Souto-Souza m.fl. (2018) hadde som målsetning å kartlegge samlet prevalens av mineraliseringsforstyrrelser blant personer med cøliaki og personer uten cøliaki. De inkluderte 45 primærstudier i en metaanalyse. Den sammenstilte evidensen indikerte at halvparten av personene med cøliaki hadde en form for mineraliseringsforstyrrelse i emaljen. Sammenlignet med kontrollpersonene i primærstudiene hadde personene med cøliaki over 130 prosent høyere sannsynlighet for mineraliseringsforstyrrelser i emaljen [52]. Forfatterne klargjorde at den biologiske mekanismen bak denne risikoøkningen til dels er ukjent, men at en mulig årsak er at personer med cøliaki kan ha begrenset mulighet til å ta opp kalsium fra kosten.
Nieri m.fl. (2017) har også evaluert prevalsen av mineralforstyrrelser for personer med cøliaki, men denne oppsummeringen vurderte barn og voksne separat, samt at risikoen for aftøs stomatitt også var et oralt utfallsmål. Prevalensestimater fra 34 primærstudier ble kombinert i en metaanalyse. For barn med cøliaki var risikoen for mineraliseringsforstyrrelser i overkant av 4,5 ganger høyere enn for barn uten cøliaki. Dette var en signifikant risikoøkning med konfidensspenn på mellom 3-8 ganger høyere risiko. For voksne personer med cøliaki ble det funnet en risikoøkning tilsvarende den estimert av Souto-Souza m.fl. (2018). Til forskjell fra den nyere metaanalysen, hadde ikke voksne en signifikant risikoøkning. For aftøs stomatitt ble det funnet en tre ganger høyere risiko hos barn med cøliaki sammenlignet med barn uten cøliaki. Det sammenstilte risikoestimatet for aftøs stomatitt blant voksne med cøliaki var på hele 47 ganger høyere risiko. Det ble derimot understreket at det var høy mulighet for skjevheter i primærstudiene, og forfatterne advarte mot å feste for mye tillit til disse estimatene [53].
NICE i England har med bakgrunn i denne sammenhengen anbefalt at personer med munnblemmer som aftøs stomatitt bør utredes for cøliaki [55].
3.2.7 Cystisk fibrose
I vårt litteratursøk identifiserte vi to oppsummeringer av moderat og høy kvalitet som studerte sammenhengen mellom cystisk fibrose og orale utfall [56]. Vi identifiserte ingen omtale av denne sammenhengen av nasjonale eller internasjonale helsemyndigheter.
Studien av Pawlaczyk-Kamieńska m.fl. (2019) var den ferskeste av studiene og hadde også høyest vitenskapelig kvalitet. Målet med oppsummeringen var å kartlegge orale manifestasjoner av cystisk fibrose basert på de siste 20 års vitenskapelige grunnlag. Det ble inkludert 13 studier som omfattet 730 personer med og uten cystisk fibrose. Av orale manifestasjoner ble emaljedefekter, karies og periodontitt undersøkt i primærstudiene. Oppsummeringen konkluderte med at det var tilnærmet lik prevalens av alvorlige emaljedefekter hos personer med cystisk fibrose sammenlignet med kontrollpersonene. Tilsvarende ble det funnet omtrent lik kariesforekomst som hos friske individer. Det var derimot ikke mulig å konkludere hvorvidt det er lik eller ulik forekomst av periodontitt hos personer med cystisk fibrose sammenlignet med friske personer [56].
Den andre oppsummeringen fokuserte spesifikt på forekomsten av karies hos barn og ungdommer under 18 år med cystisk fibrose relativt til friske.
Oppsummeringen søkte i tre databaser, fra første mulige dato frem til 2013, og kunne inkludere 15 primærstudier. Det ble forklart at det lenge hadde vært en utbredt oppfatning i miljøet for pediatrisk tannhelse at barn med cystisk fibrose har lavere risiko for å utvikle karies da de bruker kronisk antibiotika som beskytter mot kariesgenererende bakterier. Denne systematiske gjennomgangen fant at dette trolig også var tilfellet for de yngste barna med cystisk fibrose. Studien fant imidlertid at ungdommer med cystisk fibrose ikke var mer beskyttet mot karies enn ungdommer uten sykdommen [57].
3.2.8 Cerebral parese
Vi identifiserte to oppsummeringer hvor fokuset var orale manifestasjoner for personer med cerebral parese. Etter vurdering av kvaliteten ble én vurdert mangelfull da det ikke var mulig å etterprøve hvordan litteratursøket var innrettet.
Den andre oppsummeringen holdt høy kvalitet og ble gjennomført i 2018 [58]. Målet med denne var å gjennomgå all publisert data på sikling, svelge- og spiseproblemer hos personer med cerebral parese gjennom livet, og sammenstille estimater på prevalensen av disse orale manifestasjonene ved metaanalyse. Det ble inkludert 42 primærstudier med observasjoner for over 23 000 personer med cerebral parese. Prevalensen ble ikke vurdert opp mot kontrollgrupper. Sialoré ble funnet å forekomme hos 44 prosent av de inkluderte, og svelgevansker hadde en samlet prevalens på 50 prosent. Problemer med å spise ble estimert til å forekomme hos over 53 prosent av personene med cerebral parese.
Sammenhengen mellom cerebral parese og sialoré ble funnet diskutert av både Helsedirektoratet og NICE i England. Utover det faktum at tilstandene er assosiert anbefaler NICE at barn med denne utfordringen kan vurderes for legemiddelbehandling med preparater med antikolinerg effekt [59].
3.2.9 Hepatitt C
Vi identifiserte to oppsummeringer som tok for seg oral lichen planus-forekomst hos personer med hepatitt C-infeksjon [60, 61].
Den ferskeste av disse var Alaizari m.fl. (2016) som søkte etter litteratur publisert mellom 2005 og 2015 i tre databaser. Totalt 19 studier ble inkludert med over 1 800 personer. Det ble funnet at personer med oral lichen planus har seks ganger høyere sannsynligvis for å ha hepatitt C-infeksjon enn personer uten oral lichen planus.
Ti år tidligere ble sammenhengen også undersøkt av Lodi m.fl. (2004). De hadde som mål å oppsummere evidensen og teste nullhypotesen at det ikke er forskjell i prevalens av hepatitt C-virus infeksjoner mellom personer med lichen planus og friske kontrollpersoner. Publikasjonen rapporterer både en tverrsnittstudie foretatt på tre italienske klinikker som undersøkte prevalens av hepatitt C virus infeksjoner hos pasienter med lichen planus, og en systematisk gjennomgang og metaanalyse. Hovedresultatet fra metaanalysen var at personer med lichen planus hadde signifikant høyere sannsynlighet for å ha hepatitt C-infeksjon sammenlignet med kontrollpersonene. Det var derimot stor heterogenitet grunnet veldig ulik prevalens av hepatitt C generelt i ulike regioner. I subgruppeanalyser begrenset til samme geografiske områder ble denne heterogeniteten redusert. Av særlig relevans for Norge ble det funnet at personer med lichen planus i Nord-Europa ikke hadde signifikant høyere sannsynlighet for å være hepatitt C infisert sammenligner med kontrollpersonene [61].
3.2.10 Prematur fødsel
To oppsummeringer så på effekter av for tidlig fødsel på utvikling av emaljen [62, 63]. Utover oppsummeringene har vi ikke kartlagt relevant informasjon om orale manifestasjoner på prematur fødsel fra helseforvaltninger.
Bensi m.fl. (2020) undersøkte forekomsten av forstyrrelser i emaljeutvikling hos for tidlig fødte. Målsetningen var å vise en mulig assosiasjon ved sammenstilling av inkluderte observasjoner fra 13 000 barn. De fant at prematurt fødte barn hadde om lag tre ganger høyere sannsynlighet for å ha forstyrrelser i emaljeutviklingen enn barn fødte til termin. [62].
Jacobsen m.fl. (2014) undersøkte seks år tidligere hvorvidt å være født før den 37. uke er assosiert med emaljeopasitet eller emaljehypoplasi. De inkluderte 23 studier, med observasjoner for totalt 682 personer født før den 37. uke (eksponert gruppe), og ved eller senere enn den 37. uke (kontrollgruppe).
Oppsummeringens resultater indikerer at å være født før den 37. uke er assosiert med utviklingsforstyrrelser i emaljen. Det ser ut til å være en økt risiko for emaljehypoplasier i melketenner i denne gruppen og opasiteter i emalje på melketenner hos barn med veldig lav fødselsvekt. Forfatterne konkluderer at basert på deres gjennomgang er det for få høykvalitetsstudier til å fastslå sikkert hvilken assosiasjon prematur fødsel og emaljeforstyrrelser har. De pekte på at viktige konfunderende variabler som mors helse, medikamentbruk, alkohol- og kaffeinntak, samt røyking ikke var kontrollert for i alle deres inkluderte studier.
3.2.11 Hjerneslag
Hjerneslag ble utredet som både eksponeringstilstand og utfallstilstand i vårt utvalg. Vi identifiserte to studier hvor hjerneslag var eksponeringstilstanden, mens i delavsnitt 3.3.1 presenterer vi oppsummeringer der hjerneslag er utfallstilstanden.
Pillai m.fl. (2018) gjennomførte en systematisk gjennomgang på litteraturen om forholdet mellom hjerneskader og orale utfall. De fant kun referanser til hjerneslag, og underkategorier av dette (hjerneblødning og hjerneinfarkt). Totalt 30 studier ble evaluert og sortert etter studienes hypotese om årsaksforholdet. Halvparten av studiene vurderte hjerneslaget som den trolige driveren bak forholdet til orale tilstander, og den andre halvparten hadde motsatt hypotese. Dokumentasjonsgrunnlaget i oppsummeringen tillot ikke å fastslå retningen på assosiasjonene. Den hyppigste assosiasjonen var mellom hjerneslag og periodontitt. Forfatterne fremhevet at de fleste studiene på denne assosiasjonen faktisk kontrollerte for viktige felles faktorer for utvikling av tilstandene. Konklusjonen ble at det var lite evidens for at hjerneslag er en risikofaktor for periodontitt, og at det er mer sannsynlig at periodontitt er en risikofaktor for hjerneslag [64].
Dai m.fl. (2015) gjennomgikk litteraturen på orale helseutfall hos personer som har hatt hjerneslag. De undersøkte hvorvidt forekomsten av karies, og periodontale utfall som gingivitt, periodontitt og tanntap er høyere enn hos personer som ikke hadde hatt hjerneslag og ellers var friske. De sammenstilte observasjonene fra 2 100 personer i 23 studier i en metaanalyse. De fant at personer som hadde hatt hjerneslag hadde gjennomgående dårligere oral helsestatus enn kontrollpersonene, herunder signifikant færre tenner, høyere karies skår, høyere gingivittindeksskår, og høyere klinisk festetap (periodontittindikator) [65].
Helsedirektoratet har skrevet om aspirasjonsproblemer for personer som har hatt hjerneslag. De viser til studier av varierende forekomst av svelgevansker hos slagrammede fra 19-81 prosent. Aspirasjonspneumoni er den alvorligste komplikasjonen med økt risiko for død og alvorlig funksjonshemning. Videre kan svelgevansker også bidra til underernæring, men for om lag 80 prosent bedrer svelgevanskene seg i løpet av 2-4 uker [66]. Puste- og svelgevansker drøftes også i veiledere for behandling av slagpasienter av NICE i England [67] og SIGN i Skottland [68].
3.1.12 Systematiske oppsummeringer på andre generelle tilstander med orale manifestasjoner
Vi identifiserte 16 systematiske oppsummeringer hvor vi ikke fant flere enn én publikasjon på samme sammenheng. Fire av disse hadde mangelfull kvalitet.
Akcalı m.fl. (2019) undersøkte hvorvidt det er en sammenheng mellom talassemi, og gingivitt og orale blødninger. Talassemi er en relativt hyppig forekommende tilstand i middelhavslandene, India og Pakistan, og skyldes en arvelig genfeil.
Oppsummeringen undersøkte sammenhengen basert på et litteratursøk som resulterte i 16 inkluderte primærstudier med til sammen 3 300 personer. Det ble funnet signifikant forskjell i gjennomsnittlig forekomst mellom personer med talassemi og friske kontrollpersoner. Oppsummeringen konkluderte at pasienter med talassemi har signifikant høyere gjennomsnittlig forekomst av gingvalinfeksjon og orale blødninger sammenlignet med friske kontrollpersoner [69].
Kapferer-Seebacher m.fl. (2017) hadde som målsetning å vurdere orale manifestasjoner på den sjeldne sykdomsgruppen Ehlers-Danlos’ syndrom.
Litteratursøket inkluderte 43 studier på 130 personer totalt. Oppsummeringen fant at tidlig-stadium av alvorlig periodontitt er en veldig hyppig forekommende periodontal manifestasjon på Ehlers- Danlos’ syndrom. Av individene undersøkt i studiene hadde 98 prosent denne manifestasjonen [70].
Norsk helseinformatikk og Socialstyrelsen i Sverige har beskrevet på sine oversiktssider for Ehlers-Danlos’ syndrom at personer med syndromet kan utvikle både skjørhet av munnslimhinnen og stivhet av kjeveleddet etter gjentatte leddforskyvninger med blødning som kan vanskeliggjøre munnhygiene [71, 72].
Aminoshariae m.fl. (2017) ville undersøke hvorvidt personer med et utvalg systemiske sykdommer (hjerte- og karsykdommer, diabetes, kreft via bisfosfonatbehandling, og HIV) kan påvirke utfallet av rotfyllinger, som diskutert over i avsnittet for diabetes (3.2.2). Oppsummeringen holdt etter vår vurdering høy vitenskapelig kvalitet og inkluderte 16 studier på over 56 000 personer i sin kvalitative drøfting.
Forfatterne trakk en konservativ konklusjon om at all identifisert evidens var for svak for å kunne gi et godt svar på problemstillingen, og de etterlyste veldesignede longitudinelle studier på sammenhengene [73]. Relatert til HIV/AIDS forklarer Folkehelseinstituttet i sin rapport om tannhelsestatus i Norge fra 2009 at candidoseinfeksjon er relativt vanlig hos pasienter med immunsvikt, en gruppe som utgjør ca. 70 prosent av AIDS-pasientene [74].
Limeira m.fl. (2019) tok for seg en mulig sammenheng mellom kronisk nyresykdom og mineraliseringsforstyrrelser i emaljen. Et litteratursøk ble gjennomført i fire medisinske databaser med 16 inkluderte studier som resultat. Mye av oppsummeringen var en omfattende diskusjon av evidensgrunnlaget for sammenhengen mellom karies og forstyrrelser i emaljen hos personer med kronisk nyresykdom. Det ble ikke funnet noen statistisk signifikant forskjell i prevalens for disse orale utfallene mellom personer med og uten kronisk nyresykdom. Det var videre stor heterogenitet mellom primærstudienes utfall, og det er derfor noe uklart om inklusjonsprosessen var vellykket eller om det ble inkludert for ulike studier [75].
Oppsummeringen til Kellesarian m.fl. (2017) fant et positivt forhold mellom polycystisk ovariesyndrom og periodontal sykdom, basert på ti studier vurdert å ha feilfri kvalitetsvurdering. Studiene kontrollerte for relevante konfunderende variabler som medikamentbruk, orale prevensjonsmidler, hormontilsetninger, blodtrykksenkende medisiner, antibiotikabruk og antiinflammatoriske medikamenter. Til tross for dette var forfatterne varsomme med å konstatere en sammenheng og etterlyste prospektive longitudinelle studier på sammenhengen [76].
Fuertes-González m.fl. (2011) hadde som målsetning å gjennomføre en litteraturgjennomgang av sammenhengen mellom Retts syndrom og orale manifestasjoner. De inkluderte syv studier av personer med tilstanden og beskrev de orale utfallene. Ifølge oppsummeringen kan Retts syndrom gi i hovedsak to typer orale manifestasjoner. Den ene som følge av medikamentell behandling, herunder munntørrhet, stomatitt, gingivitt og dysfagi. Den andre typen kommer som en følge av sykdommen. Disse manifestasjonene kan være bruksisme og gingivitt.
Litteraturgjennomgangen klarte ikke å spesifikt slå fast hvilke orale manifestasjoner som kan tilskrives Retts syndrom, eller hvilke som oppstod tilfeldig basert på utvalget [77].
Molina-García m.fl. (2016) så også på sjeldne sykdommers orale manifestasjoner. Oppsummeringen hadde som fokus å se på funn fra litteraturen på orale tilstander hos personer med sjeldne sykdommer opp mot forekomsten av disse syndromene i Spania. De fant at personer med agammaglobulinemi hadde signifikant høyere forekomst av mineraliseringsforstyrrelser i emaljen og munntørrhet sammenlignet med friske kontrollpersoner. Personer med Retts syndrom hadde signifikant høyere forekomst av åpent frambitt, "arched palate", bruksisme og munnpusting. Personer med Prader-Willis' syndrom hadde signifikant høyere forekomst av tannerosjon.
Det ble ikke funnet noen signifikante orale forskjeller fra en normalpopulasjon for personer med cystisk fibrose. Resultatene må imidlertid tolkes som geografisk avgrensede, og det er uklart om oppsummeringen har ekstern validitet i en annen populasjon enn den spanske [78].
En annen nokså smalfokusert oppsummering av Travaglino m.fl. (2020) så på prevalensen av Sjögrens syndrom i pasienter med spyttkjertelkreft.
Litteratursøket omfattet perioden 2000-2019, og søket i fem databaser resulterte i 16 studier med observasjoner på totalt 665 pasienter med spyttkjertelkreft. Prevalensen av Sjøgrens syndrom ble sammenstilt som i en metaanalyse og ble beregnet til å forekomme hos 18 prosent av spyttkjertelkreftpasientene [79].
Orale manifestasjoner på Sjøgrens syndrom og reumatiske lidelser generelt ble beskrevet av de svenske og skotske helseforvaltningene. I Sverige løftet SBU fram erfaringer beskrevet av den svenske reumatikerforeningen om at mange med Sjøgrens syndrom opplever munntørrhet [80]. I Skottland har NHS antydet at personer reumatoid artritt kan få utfordringer med å opprettholde oral hygiene, hvilket også kan eksponere de for risiko for periodontitt [81].
Oppsummeringen til Khalighinejad m.fl. (2016) tok for seg et bredt spekter av potensielle sammenhenger mellom systemiske sykdommer og apikal periodontitt. De identifiserte åtte studier på sammenhengen mellom hjerte- og karsykdom og periodontitt. Syv av disse rapporterte et signifikant forhold, mens én fant ingen slik assosiasjon. Forfatterne av oppsummeringen konkluderer med at det kan være en sammenheng, men at denne må tolkes forsiktig. Videre fant de tre studier som rapporterte om en sammenheng mellom periodontitt og diabetes. Artiklene ble imidlertid funnet å ha store skjevheter, det ble derfor konkludert med at evidensen ikke var tydelig. For sammenhengen med kronisk leversykdom ble det funnet én studie.
Denne rapporterte høyere risiko for apikal periodontitt for pasientene med leversykdom enn for friske, men det ble ikke kontrollert for konfunderende variabler. Til slutt fant oppsummeringen én studie på sammenheng mellom apikal periodontitt og lav beintetthet. Det ble rapportert om en statistisk signifikant sammenheng, men ikke kontrollert for noen variabler som alder, røyking og alkohol, eller andre medisinske tilstander som også er karakterisert ved lav beintetthet [82].
Den siste oppsummeringen på en sammenheng mellom somatisk sykdom og orale utfall med kun ett treff i vårt søk var Guo m.fl. (2017). De ønsket å fastsette hvilken søvnrelatert adferd som er risikofaktorer for bruksisme hos barn under 13 år. Litteratursøket gav 14 primærstudier med over 14 000 barn som enten snorket, var munnpuster, sov urolig, siklet, sov på magen eller som slet med søvnmangel, samt barn uten slik søvnadferd. Resultatene ble sammenstilt i en metaanalyse for å estimere risiko for bruksisme relativt til barn uten søvnproblemer. Barn som snorket hadde omtrent 2,5 ganger høyere risiko for bruksisme enn kontrollpersonene. Barn som var munnpustere hadde 50 prosent høyere risiko, barn som siklet hadde omtrent 80 prosent høyere risiko, og for de som generelt sov urolig var det en 130 prosent høyere risiko for bruksisme. Samtlige av disse estimatene var statistisk signifikant høyere enn hos kontrollpersonene [83].