Fagbegrep i delkapitlet:
- Dental agenesi Fravær av én eller flere tenner.
- Dental- og emaljehypoplasi Utviklingsforstyrrelser av emaljen.
- Osteoradionekrose Nedbrytning av bensubstans som følge av radiologisk behandling (strålebehandling).
- Trismus Gapebesvær, eller kjevesperre.
Fra litteratursøket fant vi flest treff på sammenhengen mellom behandling for kreft og orale bivirkninger som påvirket den orale helse. Fra søkene i forvaltningskildene fant vi også omtale av hvordan behandling for andre somatiske tilstander var assosiert med orale tilstander. I Figur 3-6 viser vi en grafisk fremstilling av funn fra litteratursøket, der behandling for somatisk sykdom (eksponeringsfaktor) er gjengitt til venstre i figuren og orale tilstander assosiert med behandlingen (utfallet) er vist til høyre i figuren. Av Figur 3-6 fremgår det at strålebehandling i forbindelse med kreft var den behandlingen for somatisk sykdom som var tema i flest oppsummeringer, etterfulgt av bisfosfonatbehandling (i forbindelse med kreft og for andre diagnoser enn kreft) og kjemoterapi i forbindelse med kreft.
Figur 3-6 Studerte sammenhenger i systematiske oversikter identifisert som beskrivende for behandling for somatisk sykdom som kan påvirke den orale helse
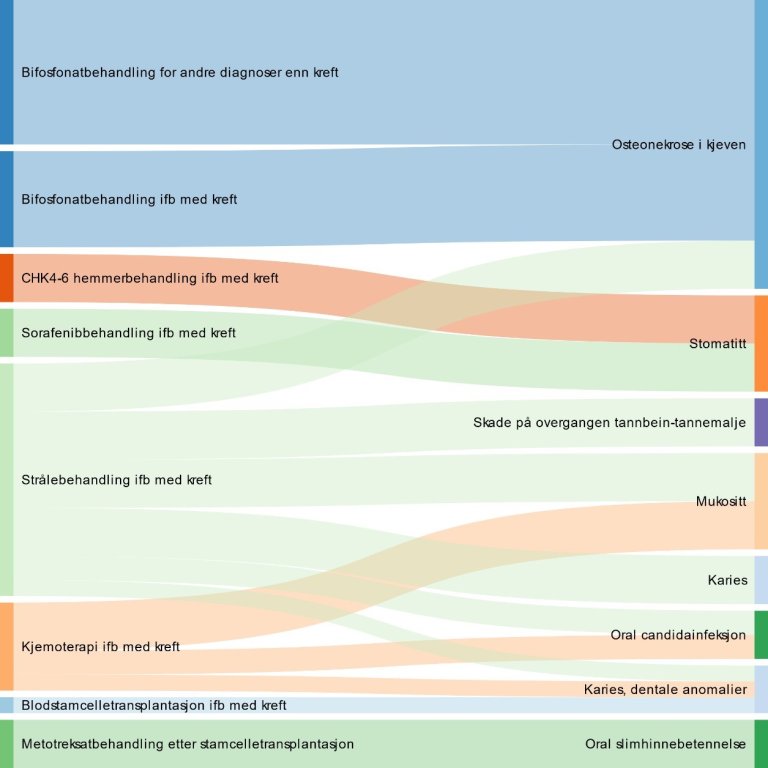
3.4.1 Strålebehandling i forbindelse med kreftdiagnose
VI identifiserte seks studier på orale utfall etter strålebehandling for kreft [121-126]. Orale tilstander som kan følge av strålebehandling for kreftpasienter har også blitt beskrevet av helseforvaltningene i Norge, Sverige, Danmark og Skottland. I Danmark har Sundhedsstyrelsen utarbeidet nasjonale kliniske retningslinjer, pakkeforløp for hode- og halskreft, og et oppfølgingsprogram etter hode- og halskreftbehandling, samt en rapport som har samlet vitenskapelig litteratur om senfølger etter stråleterapi mot kreft hos voksne.
Stråling mot hoderegionen og karies ved kreftbehandling
Vi identifiserte to oppsummeringer som beskrev sammenhengen mellom strålebehandling for hode-, nakke-, og halskreft og karies [122-123]. Begge fant en høyere risiko for å utvikle karies blant pasienter som behandlet med stråling.
Den nyeste oppsummeringen, Moore m.fl. (2020), undersøkte forekomsten av nye kariestilfeller etter strålebehandling for hode- og nakkekreftpasienter. Kariesforekomsten ble funnet å øke over tid. Ved sammenstilling av dataene fra to-års oppfølging etter stålingen ble det fastsatt omtrent 40 prosent hadde karies. Sammenstillingen var derimot understøttet av studier med betydelige forskjeller. Forfatterne advarte derfor mot at resultatene kunne være påvirket av disse forskjellene [122].
Hong m.fl. (2010) fant i tillegg at karies var mer hyppig blant pasienter som kun hadde gjennomgått kjemoterapi enn pasienter som hadde gjennomgått både kjemoterapi og strålebehandling, eller bare strålebehandling. Dette ble beskrevet som et overraskende funn. Forfatterne framsatte en hypotese om at det kan være større bevissthet rundt orale bivirkninger av strålebehandling hos behandlerne, slik at pasientene kan ha fått bedre tannlegeoppfølging. En alternativ forklaring er at de fleste primærstudiene så på utfall hos barn (12/19 studier). Barn kan ha høyere risiko for karies ved kreftbehandling fordi de ofte er syke lenge og krever høykalorikost for å holde vekten, eller fordi de ordineres sukroserike legemidler [123].
Stråling mot hoderegionen og andre orale utfall ved kreftbehandling
Vi identifiserte fire oppsummeringer som så på hvordan strålebehandling for pasienter med hode- og halskreft påvirket forekomst og risiko for dentale sykdommer [124-127]. Samtlige kom frem til at strålebehandling mot hoderegionen bidrar til økt risiko for dentale sykdommer. Det ble også funnet omtalte sammenhenger i forvaltningskilder fra både Danmark, Norge og Sverige.
Den nyeste oppsummeringen, Fonseca m.fl. (2020), studerte seneffekter av stråling, herunder karies og dentale utviklingsanomalier. De undersøkte hvorvidt ioniserende stråling skader mikromorfologiske egenskaper i overgangen mellom tannbein og emalje, og om dette bidrar til å progrediere allerede manifestert karies. Det ble konkludert at strålebehandling ved hode- og halskreft kan være en uavhengig risikofaktor for karies og dentale utviklingsanomalier. Konklusjonen var derimot understøttet av studier med små utvalg og sprikende metodologisk tilnærming. Det er derfor noe usikkerhet i hvor stor grad stråling mot hoderegionen gir dentale seneffekter [124].
Gawade m.fl. (2014) inkluderte også studier som så på dentale seneffekter av strålebehandling, i tillegg til kjemoterapi. De rettet fokus på personer som hadde blitt behandlet for kreft som barn. Basert på 47 studier fant de at personer som i barneårene hadde gjennomgått stråle- og kjemoterapibehandling, alene eller i kombinasjon, hadde høyere risiko for dental agenesi, dental- og emaljehypoplasi, samt underutviklede tannrøtter. Risikoen var høyere for personer med yngre alder på behandlingstidspunktet, sterkere strålingsintensitet, og ved kombinasjon av flere typer kreftbehandling [125].
I oppsummeringen til Lalla m.fl. (2010) var fokuset på forekomsten av orale soppinfeksjoner (candidoseinfeksjon) som bivirkning av kreftbehandling. Målinger fra 160 pasienter i fire studier ble presentert i oppsummeringer. Før kjemoterapi hadde hele 47 prosent av pasientene en slik soppinfeksjon. Dette økte til 73 prosent mens pasientene var under aktiv behandling. Etter avsluttet kjemoterapikur hadde fortsatt 69 prosent en oral soppinfeksjon. Tilsvarende fant de at 50 prosent av i alt 110 kreftpasienter hadde candidoseinfeksjon før strålebehandling, 74 prosent under behandling, og 71 prosent etter behandling. Selv om det var økt forekomst av candidoseinfeksjon ved begge behandlingene var det ikke mulig å utelukke tilfeldigheter da konfidensintervallene overlappet [126]. Økningen av soppinfeksjon blant pasientene under behandling ble forklart å trolig kunne tilskrives at behandlingen er assosiert med nedsatt spyttproduksjon. Dette gir munntørrhet og eksponerer derfor lettere for infeksjoner.
Trotti m.fl. (2003) fant i sin gjennomgang av litteraturen at insidensen av oral mukositt blant pasienter som mottok stråleterapi for hode- og nakkekreft var hele 80 prosent. Mukositt er derfor en av de vanligste bivirkningene ved strålebehandling mot hoderegionen. Målet med oppsummeringen var å etablere hvorvidt mukositt kunne forklare sykehusinnleggelser og ulike kliniske utfall. Basert på erfaringene fra 700 pasienter behandlet med og uten stråling, ble det funnet en betydelig høyere andel (32 prosent) innleggelser for mukositt blant de strålebehandlede, enn de som ikke mottok stråling (5 prosent). Oppsummeringen gjennomførte også parvis korrelasjonsberegning mellom mukositt og kliniske utfall, herunder vekttap og innsetting av magesonde. Alvorlig mukositt hadde 88 prosent korrelasjon til vekttap, og 83 prosent korrelasjon til behov for magesonde [127]. Selv om begge korrelasjonene var signifikante gir enkle korrelasjoner et unyansert bilde, og det er alltid en risiko for at korrelasjonene kun samvarierer tilfeldig.
Sundhedsstyrelsen i Danmark har utviklet et pakke- forløp for hode- og halskreft som omhandlet oppfølging etter strålebehandling. Pakkeforløpet beskrev orale tilstander som protesetilpasning, karies og osteoradionekrose og andre tann-/kjeverelaterte problemer som følger av kirurgisk og onkologisk behandling. Insidensen av osteoradionekrose etter strålebehandling varierte etter hvordan kontrollgruppene var definert i de inkluderte studiene. En inkludert oppsummering fant at opptil åtte prosent av strålebehandlede pasienter utviklet osteoradionekrose i ettertiden [128]. I pakkeforløpet understrekes det at pasienter som har blitt strålebehandlet etter denne behandlingen avsluttes anbefales livslang forebyggingsinnsats for å unngå orale seneffekter. I henhold til rapporten gjennomføres dette av pasientens tannlege. Pasienter som ikke gjennomgår stråling anbefales allikevel kontroll og forebygging hos sin tannlege tidlig etter kreftbehandlingen.
I en annen rapport beskrev Sundhedsstyrelsen at strålebehandling mot hode også kan gi en rekke andre senfølger. Disse inkluderte xerostomi, svelgeproblemer, talevansker, smaksforstyrrelser, trismus og karies [129].
I Norge har FHI beskrevet at stråling kan gi symptomer i munnen gjennom xerostomi, økt spyttmengde, smaksforstyrrelser, stomatitt, opportunistiske infeksjoner, pigmentering av munnslimhinne og tenner, hevelser, økt kariesforekomst, gingival hyperplasi og osteonekrose i kjeven [74].
I Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av pasienter med lymfomer, utarbeidet av Helsedirektoratet, var det beskrevet ulike orale tilstander som kan oppstå etter stråleterapi. Det var presisert at stråleterapi mot munnhule kan gi xerostomi og økt hyppighet av karies og tannkjøttsykdommer [66].
Strålebehandling for kreft og andre dentale sykdommer
Vårt litteratursøk kunne ikke identifisere noen oversikter som så på andre orale utfall av strålebehandling enn de som er allerede nevnt. Vi fant derimot flere omtaler av dentale utfall av stråling i forvaltningskildene.
I Helsedirektoratets retningslinjer for diagnostikk, behandling og oppfølging av kreft hos barn, ble dentale sykdommer som er forbundet med stråling og kjemoterapi beskrevet. Disse inkluderte skade på tenner under utvikling på behandlingstidspunktet, emaljedefekter, rotforkortelser, skjev tannstilling, forstyrret tann- utvikling, hull i tennene, og redusert spyttproduksjon [130].
I NHS Scotland har egne retningslinjer for diagnostikk og behandling av mukositt som har oppstått hos barn og unge personer som mottar kreftbehandling, men også ved blodstamcelletransplantasjon [131].
3.4.2 Bisfosfonatbehandling og osteonekrose i kjeven
Vi identifiserte fire oversikter som undersøkte hvorvidt pasienter behandlet med bisfosfonat hadde økt risiko for utvikling av osteonekrose i kjeven [138-141].
Lee m.fl. (2014) hadde som mål å etablere hvorvidt pasienter som ble behandlet med bisfosfonat for forebygging av osteoporose grunnet andre diagnoser enn kreft, også hadde forhøyd risiko for osteonekrose i kjeven. Hos kreftpasienter behandlet med bisfosfonat har man kjent til koblingen til osteonekrose i kjeven siden 2003. Fram til denne oppsummeringen hadde det ikke vært påvist det samme for andre diagnoser enn kreft. Metaanalysen fant at i ni studier av pasienter behandlet med bisfosfonat for andre diagnoser enn kreft var det 2-3 ganger økning i risiko for osteonekrose i kjeven sammenlignet med pasienter som ikke mottok bisfosfonatbehandling [132].
Chamizo Carmona m.fl. (2013) fant ikke at bisfosfonatbehandling økte risikoen for osteonekrose i kjeven når behandlingen var gitt alene for å forebygge osteoporose. Forfatterne pekte på at det trolig var flere faktorer som bidro til osteonekrose i kjeven. De hypotiserte at det sannsynligvis var vanlig å behandle disse pasientene med flere legemidler samtidig med bisfosfonat, slik at bisfosfonat sammen med multifarmasi kunne forklare noe av forekomsten av osteonekrose i kjeven [138].
Mauri m.fl. (2009) undersøkte den samme sammenhengen hos brystkreftpasienter. Fra metaanalysen av randomiserte forsøk fant de at osteonekrose i kjeven, som følge av bisfosfonatbehandling, var en sjelden bivirkning. Kun 13 av 5 312 pasienter utviklet tilstanden, og samtlige ble behandlet med zoledronsyre (én av fem godkjente bisfosfonatpreparater i Norge). Forfatterne konkluderte at osteonekrose kan oppstå som følge av denne behandlingen for brystkreft. Derimot er osteonekrose i kjeven nokså sjelden hos de behandlet med zoledronsyre slik at denne er å regne som trygg [134].
En eldre studie av Hess m.fl. (2008) undersøkte hvilke øvrige faktorer som var assosiert med osteonekrose i kjeven blant personer behandlet med bisfosfonat. I tillegg til at osteonekrose i kjeven kan oppstå som følge av bisfosfonatbehandling hos kreftpasienter, fant forfatterne at dette også var tilfellet for pasienter med Paget’s sykdom og reumatoid artritt. Oppsummeringen fant også at det var vanlig at disse pasientene hadde blitt behandlet med flere legemidler samtidig som bisfosfonat. Det ble understreket at osteonekrose i kjeven ikke opptrådde hos pasienter som ellers var ved god helse og ble behandlet med bisfosfonat, og at det trolig er flere faktorer som bidrar til tilstanden [135].
Bisfosfonatbehandling og dentale tilstander
Andre dentale tilstander som kunne følge av behandling med bisfosfonat mot osteoporose ble omtalt i et informasjonsskriv rettet mot pasienter utarbeidet av NICE i England. I informasjonsskrivet ble blemmer på spiserøret nevnt som en mindre vanlig, men alvorlig sideeffekt av injeksjon med bisfosfonat [136].
Kjemoterapi i forbindelse med kreft og stomatitt
Lasheen m.fl. (2017) undersøkte i sin metaanalyse hvorvidt brystkreftpasienter behandlet med CDK4-6 hemmere hadde økt risiko for forekomst av stomatitt. De fant at behandling med CDK4-6 hemmere økte risiko for stomatitt med nesten 400 prosent (50 av 428 behandlede pasienter fikk stomatitt mot seks av 249 kontrollpersoner). Av de to tilgjengelige CDK4-6 hemmerne var det kun palbociclib som var studert [137].
Abdel-Rahman og Fouad (2014) gjennomførte en lignende analyse for pasienter med solide tumorer behandlet med sorafenib. De undersøkte bivirkningen av behandlingen opp mot kontrollpersoner behandlet med placebo, eller standard kjemoterapi (gemcitabin/cisplatin). Relevant for denne rapporten var forekomsten av stomatitt. Ni studier med observasjoner for 3 400 personer ble inkludert i metaanalysen. Pasientene behandlet med sorafenib hadde 190% høyere sannsynlighet for å få stomatitt som bivirkning enn de behandlet med standard kjemoterapi, eller placebo [138].
Kjemoterapi i forbindelse med kreft og dentale tilstander
Det var tre eldre studier fra vårt utvalg som undersøkte dentale lidelser som følge av behandling med kjemoterapi [122, 125-126]. Én studie er tidligere beskrevet i delavsnitt 3.4.1 [122].
Gawade m.fl. (2014) studerte forekomsten av dentale utfall for personer som i barndommen ble behandlet for kreft med stråling, og/eller kjemoterapi, eller mottatt blodstamcelletransplantasjon. Det var ikke mulig å knytte de dentale utfallene til enten stråling eller kjemoterapi for personene behandlet for kreft. Denne oppsummeringen gjorde ingen etterberegning for å sammenstille forekomsten av utfallene i de ulike studiene. Karies var et relativt vanlig forekommende utfall etter kreftbehandlingen. Én beskrevet studie fant at etter 2,5 år etter behandlingen hadde over 80 prosent av barna karies. Hos barn i den friske kontrollgruppen var forekomsten om lag 50 prosent. En dansk studie inkludert i oppsummeringen kunne derimot påvise at kariesforekomsten faller og nærmer seg forekomsten hos friske på senere oppfølgingstidspunkt (7, 12 og 15 år etter behandling). Det ble også funnet sterk evidens for at særlig kjemoterapi kan være assosiert til høyere risiko for dental agenesi, dental- og emaljehypoplasi, samt underutviklede tannrøtter. For barn behandlet med blodstamcelletransplantasjon fant oppsummeringen at karies var rapportert både lik som hos friske kontrollpersoner, og høyere enn forekomsten hos disse. Oppsummeringen beskrev at barn behandlet med blodstamcelletransplantasjon og kjemoterapi hadde ved to-års oppfølging signifikant flere tenner med underutviklede røtter enn de som mottok kun kjemoterapi [125].
Hong m.fl. (2010) beskrev en høyere kariesprevalens hos pasienter som kun hadde gjennomgått kjemoterapi enn både kjemoterapi og strålebehandling eller bare strålebehandling. Oppsummeringen trakk fram mulige forklaringsårsaker til funnene. En økt bevissthet rundt orale bivirkninger av strålebehandling hos behandlere kan være en årsak. I denne oppsummeringen hadde de fleste studiene sett på kariesprevalens hos barn.
Det ble framsatt at barn også kan ha høyere risiko for karies da de er syke lengre, og har behov for høykalorikost for å holde vekten eller at de ordineres sukroserike legemidler [123].
Lalla m.fl. (2010) kunne notere en økt risiko for oral soppinfeksjon forbundet med kreftbehandling. Fire av studiene fulgte kreftpasienter før og etter kjemoterapibehandling. Andelen med candidoseinfeksjoner under og etter kjemoterapibehandling (30-40 prosent) var markant høyere enn før behandlingen (7,5 prosent). De fant også tilsvarende økende mønster i candidainfeksjon ved strålebehandling [126].
Kjemoterapi i forbindelse med kreft og mukositt
Oral mukositt som følge av kjemoterapibehandling for kreftpasienter var derimot beskrevet i forvaltningskilder fra England og Skottland og Sverige.
NICE i England har utarbeidet to retningslinjer som omtaler oral mukositt som en vanlig sideeffekt av kjemoterapi henholdsvis for kjemoterapi/radioterapi i behandling av hode- og nakkekreft [139] og ved spesifikk 5-FU kjemoterapi [140].
I Skottland har SIGN publisert kliniske nasjonale retningslinjer for langtidsoppfølging av kreftoverlevere som barn. I retningslinjene er det beskrevet studier som er gjennomført for å undersøke effekten av å motta kreftbehandling som barn på dental utvikling. Det ble beskrevet at studiene konsistent demonstrerte forstyrrelser i mineraliseringen og utviklingen av kroner og tannrøtter.
Sannsynligheten for dentale problemer senere i livet var større dess yngre pasientene var på tidspunktet for behandlingen [141].
Kjemoterapi i forbindelse med kreft og xerostomi
Helsedirektoratet har utarbeidet to nasjonale handlingsprogram som har omtalt sammenhengen mellom kjemoterapi i forbindelse med kreft og xerostomi. Fra Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av bukspyttkjertelkreft omtales xerostomi som et av flere vanlige symptomer ved symptomrettet palliativ behandling hos pasienter med bukspyttkjertelkreft [142]. I det andre handlingsprogrammet, som beskriver retningslinjer for palliasjon i kreftomsorgen, er xerostomi omtalt som en svært hyppig bivirkning hos palliative pasienter, mens hypersalivasjon var sjeldnere hos kreftpasienter, men kunne være et stort problem ved visse nevrologiske sykdommer [130, 143]. Det digitale medisinske oppslagsverket, Norsk helseinformatikk, har også beskrevet xerostomi som et svært plagsomt symptom hos mange kreftpasienter, i tillegg til såre og skjøre slimhinner, hvor det lett kan oppstå infeksjoner og gjøre det vanskelig å spise og svelge [144].
Sundhedsstyrelsen i Danmark har også omtalt xerostomi som det hyppigste problemet ved rutinekontroll av pasienter med hode- og halskreft og en betydelig andel av pasientene har opplevd alvorlig xerostomi [145].
3.4.3 Øvrig behandling for somatisk sykdom med orale bivirkninger
To oppsummeringer i vårt utvalg tok for seg sammenhengene mellom øvrig behandling for somatisk sykdom og orale bivirkninger [143, 125]. Denne assosiasjonen var også omtalt i flere forvaltnings- dokumenter fra både Skottland, Norge, Danmark og England.
To studier fra vårt utvalg studerte orale tilstander som følge av gjennomgått behandling med stamcelletransplantasjon [125, 148]. Studiene konkluderte med at det var økt risiko for utvikling av dentale sykdommer senere i livet. Denne risikoen økte ved mer intensiv behandling eller dersom pasienter hadde mottatt strålebehandling og høy-dose kjemoterapi før blodstamcelletransplantasjonen. Fra studien som så på langtidseffekter av blodstamcelletransplantasjon var evidensen på karies motstridende [125].
En oppsummering av Chaudhry m.fl. (2016), undersøkte forekomst og alvorlighetsgrad av oral mukositt blant pasienter som har gjennomgått stamcelletransplantasjon, med fokus på assosiasjonen med intensiteten av tilpasningsbehandling. De beskrev en signifikant høyere forekomst av alvorlig oral mukositt hos pasienter som gjennomgikk mer intensiv tilpasningsbehandling, herunder profylaktisk behandling med metotreksat [146].
NHS Scotland har fremlagt kliniske pediatriske retningslinjer for diagnostikk og behandling av mukositt som har oppstått hos barn og unge personer som mottar kreftbehandling, særlig i tilfeller ved blodstamcelletransplantasjon. Orale komplikasjoner som kan følge av behandlingen er smerte, dysfagi, talebesvær og problemer med oralt inntak av ernæring [131].
Helsedirektoratet har i de nasjonale faglige retnings- linjene og veiledere for forebygging, diagnostisering og oppfølging av kols rapportert om mulige bivirkninger av behandling med tiotropium, blant annet xerostomi. Videre har bruk av inhalasjonssteroider blitt beskrevet som legemiddel som kan gi tendens til soppinfeksjon i munnhulen.
Sundhedsstyrelsen i Danmark har utviklet et anbefalingsskriv for tverssektorielle forløp for mennesker med kols, der xerostomi trekkes frem som en typisk langtidsbivirkning av basisbehandling mot kols.
Behandling for søvnapné, spasmer, ikke-hormonelt alternativ ved østrogenmangel og orale bivirkninger
NICE i England og Helsedirektoratet har utviklet retningslinjer for somatisk tilstand, herunder søvnapné, behandling med botulinum type A, og behandling med clonidin, og omtalte orale bivirkninger.
I England har NICE utarbeidet to retningslinjer som har omtalt orale bivirkninger av behandling for søvnapné og injeksjon for behandling mot spasmer [147]-[148]. Xerostomi var rapportert blant flere pasienter innen tre år etter behandlingstidspunktet for hypoglossal nervestimulering for moderat til alvorlig obstruktiv søvnapné [147]. Behandling med botulinum type A injeksjon mot spasmer ved cerebral parese hos barn og unge kunne medføre sjeldne, men alvorlige komplikasjoner som svelgevansker, og i noen tilfeller også pustebesvær [148].
Helsedirektoratet publiserte nylig nasjonale retnings- linjer for diagnostikk, behandling og oppfølging av pasienter med brystkreft. Blant de ikke-hormonelle alternativene for behandling ved østrogenmangel- symptomer etter brystkreft har clonidin blitt nevnt, og kjente bivirkninger som kan opptre er særlig xerostomi [149].
3.4.4 Behandling for psykisk sykdom med orale bivirkninger
Sundhedsstyrelsen i Danmark har i sitt veiledningsprogram for schizofreni beskrevet hvordan antikolinergika kan motvirke ekstrapyramidale bivirkninger (EPS), men at behandlingen også kan ha flere bivirkninger som xerostomi og nedsatt kognitiv funksjon [150]. National Institute for Health and Care Excellence i England har i en kunnskapsoppsummering også nevnt xerostomi som en potensiell oral bivirkning av behandling mot generalisert angstsykdom [151].
I Norge har Helsedirektoratet utarbeidet nasjonale faglige retningslinjer for utredning, behandling og oppfølging av personer med psykoselidelser, der redusert spyttmengde trekkes frem som en vanlig bivirkning av antidepressiva. I tillegg til munntørrhet nevnes også økt risiko for hull i tennene samt infeksjoner i munnhulen og dårlig ånde som mulige orale bivirkninger [152].
En utredningsrapport av SBU i Sverige, har beskrevet hvordan psykiatripasienter ofte har store problemer med tennene på grunn av medisinering med legemiddel som fører til xerostomi og dårlig munnhygiene [80].