Monoterapi
Adjuvant behandling med 5-fluorouracil (5-FU) bedrer 5-års sykdomsfri overlevelse ved stadium II (2–4 %) og stadium III (10–15 %) tykktarmskreft (Dahl, 2007; Francini et al., 1994; Glimelius et al., 2005; O'Connell et al., 1997). Bedring i total overlevelse etter fem år er ca. 2 % ved stadium II (Figueredo et al., 2004) og 7–8 % ved stadium III (Gill et al., 2004). En meta-analyse viste ingen forskjell i sykdomsfri overlevelse i stadium II hos de som fikk adjuvant kjemoterapi eller ikke, mens det var en forskjell på 10 % til fordel for adjuvant kjemoterapi i stadium III (Böckelman et al., 2015). Perorale pyrimidiner som kapecitabin er vist å være like effektive adjuvant som intravenøs 5-FU/folinat (Lembersky et al., 2006; Twelves et al., 2005).
Sirkulerende tumor DNA (ctDNA) og digital patologi og kunstig intelligens har vist seg å bedre prognostisering og kan antakelig bidra til bedre seleksjon av pasienter som har nytte av adjuvant kjemoterapi, men metodene er foreløpig ikke i rutinemessig bruk i Norge (Kleppe et al., 2022; Tie et al., 2019).
Kombinasjonsbehandling
Tillegg av oksaliplatin til 5-FU, bedrer sykdomsfri overlevelse etter tre år fra 73 til 78 % (stadium II og III sett under ett) (André et al., 2004). Etter ti år ses en bedring i totaloverlevelse fra 59 til 67,1 % for stadium III, men ingen effekt for stadium II (79,5 % uten og 78,4 % med oksaliplatin) (André et al., 2015). Kombinasjonen kapecitabin og oksaliplatin (CAPOX) bedrer også overlevelsen sammenlignet med 5-FU monoterapi (Schmoll et al., 2015), og det er vist at CAPOX er likeverdig med FOLFOX6 (Pectasides et al., 2015). Hverken irinotekan, bevacizumab eller cetuximab gir tilleggsgevinst ved adjuvant behandling (Dahl, 2007; Saltz et al., 2007; Van Cutsem et al., 2009).
Behandling av eldre
Eldre pasienter er gjennomgående underrepresentert i studier på adjuvant kjemoterapi ved coloncancer. Nytten av slik behandling må imidlertid anses dokumentert også for eldre pasienter (Sargent et al., 2001). Toleransen er overveidende god, framfor alt for monoterapi med 5-FU eller kapcitabin.
Data tyder på at tillegg av oksaliplatin til 5-FU eller kapecitabin i adjuvant setting i liten grad bedrer overlevelsen hos pasienter over 70 år (André et al., 2004; André et al., 2015; Sargent et al., 2001)(Haller et al 2015). I denne aldersgruppen anbefales for de fleste derfor monoterapi med 5-FU eller kapecitabin.
Pasienter over 75 år bør vurderes individuelt basert på allmenntilstand, funksjonsnivå, komorbiditet og polyframasi. Onkogeriatrisk vurdering kan bidra til bedret seleksjon av pasienter.
Tidspunkt for oppstart
Flere retrospektive analyser viser at det er viktig at behandlingen starter uten unødige forsinkelser, helst innen 4–6 uker etter operasjon og senest innen 8 uker (Berglund et al., 2008; Biagi et al., 2011; Des Guetz et al., 2010a; Hershman et al., 2006; Sun et al., 2016; Yu et al., 2013).
Varighet av behandlingen
Det er ikke vist bedre overlevelse ved lengre behandling enn 6 måneder (Des Guetz et al., 2010b; Neugut et al., 2006). Hvis oxaliplatin må seponeres på grunn av bivirkninger, bør man fortsette man med 5-FU eller kapecitabin til man har gitt det planlagte antall kurer. Avbrudd av oksaliplatin etter 3 md ser ikke ut til å føre til dårligere prognose, dersom 5-FU kontinueres til 6 md (Gallois et al., 2023).
For å undersøke varighet av adjuvant behandling er det publisert resultater fra et stort internasjonalt samarbeid (IDEA collaboration) ved sammenslåing av seks studier som undersøkte 3 versus 6 md. CAPOX eller FOLFOX (André et al., 2020a; Grothey et al., 2018). Oppdaterte overlevelsesdata ble publisert i 2020. Hovedkonklusjonen er at 3 md. ikke er likeverdig 6 md., men forskjellen i overlevelse er <1% (74,6 vs 75,5 % 3-års sykdomsfri overlevelse og 82,4 vs 82,8 % 5-års totaloverlevelse) for hele gruppen. Hovedeffekten hentes ut de 3 første månedene.
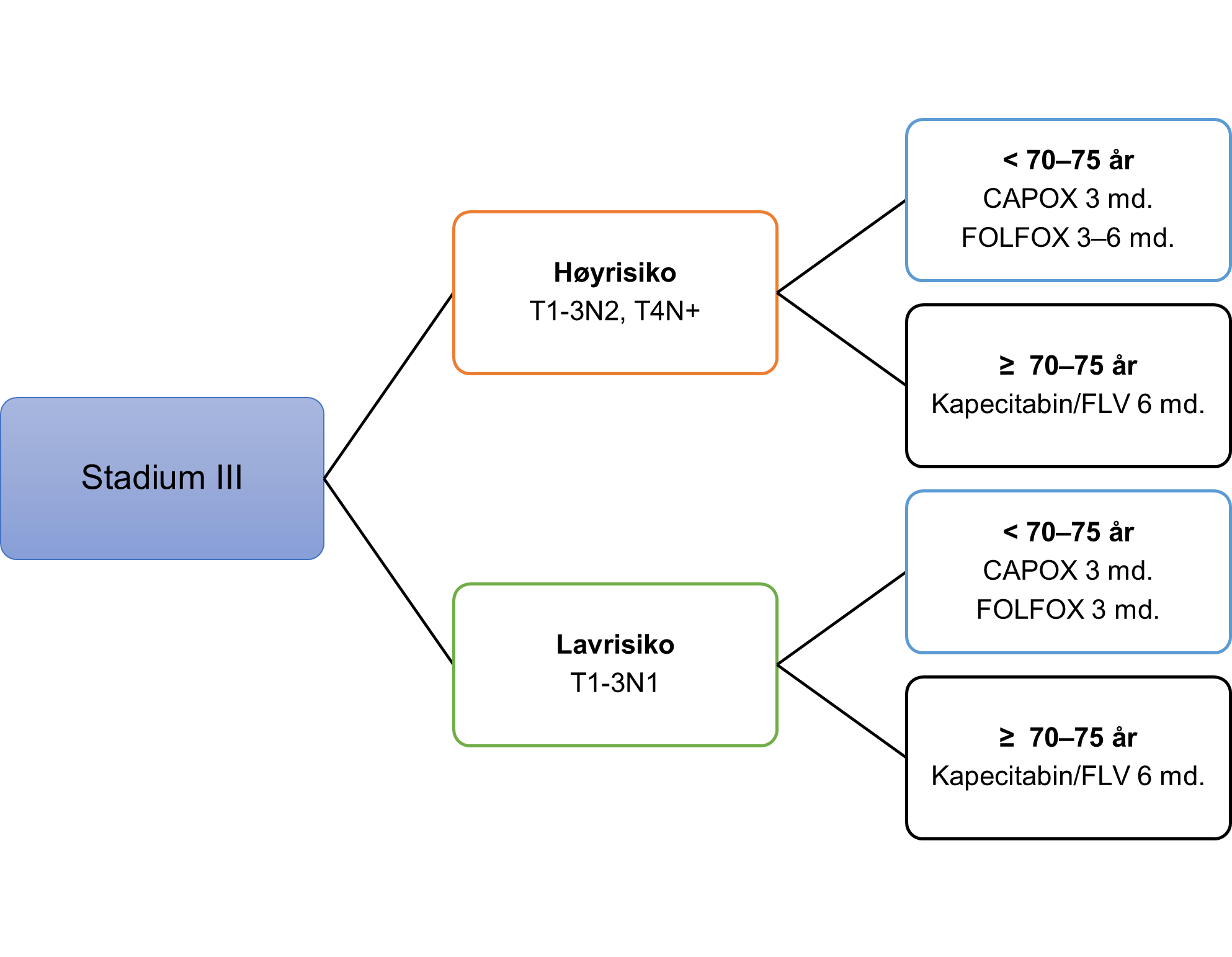
Adjuvant behandling ved stadium III
Videre er det gjort subgruppeanalyser mellom de to regimene og lavrisiko (T1-T3N1) og høyrisiko sykdom (T4N+ og N2). Ved bruk av CAPOX var det ingen reduksjon i sykdomsfri overlevelse eller totaloverlevelse for gruppen som helhet eller pasienter med lavrisiko sykdom ved 3 versus 6 md. behandling. Ved høyrisiko sykdom ble det sett økt 5 års sykdomsfri overlevelse på 2,6 % (55,6 vs 58,2 %) og 5-års overlevelse på 1 % (71,4 vs 72,4 %) ved bruk av 6 md. behandling. Denne marginale forskjellen gjør at 3 md. behandling med CAPOX kan anses tilstrekkelig også ved høyrisiko. Ved bruk av FOLFOX var det observert økt 5-års overlevelse på 1,2 % (82,6 vs 83,8 %) for hele gruppen. Forskjellen er betydelig mindre for lavrisiko gruppen (5 års sykdomsfri overlevelse 76,6 vs 79%, 5-års overlevelse 89,1 vs 89,4 %) enn for høyrisikogruppen (5-års sykdomsfri overlevelse 55,8 vs 60,8 %, 5-års overlevelse 72,5 vs 75,5 %). For pasienter i lavrisikogruppen kan derfor 3 md. FOLFOX anses tilstrekkelig.
Det er klar forskjell i oksaliplatinindusert nevropati mellom gruppene. Risikoen for nevropati grad 2 eller høyere er betydelig lavere etter 3 md. (14–16 %) sammenlignet med 6 md. behandling (45–48 %).
Oppsummert er det like god effekt ved å behandle i 3 md. for lavrisiko-gruppen (T1-3N1), best dokumentert for CAPOX. CAPOX oppleves som noe mer toksisk enn FOLFOX. Ved høyrisiko (T4 eller N2) bør man behandle 6 md. ved bruk av FOLFOX. Det er en marginal ekstragevinst å øke behandlingslengden fra 3 til 6 md. ved bruk av CAPOX. Denne gevinsten bør dog vurderes mot økt risiko for nevropati, og avgjørelsen bør tas i samvalg med pasienten. Ved neurotoksisitet kan videre behandling gis uten oksaliplatin.
Dersom det gis monoterapi med 5FU eller kapecitabin, er standard 6 md. behandling.
Adjuvant behandling ved stadium II
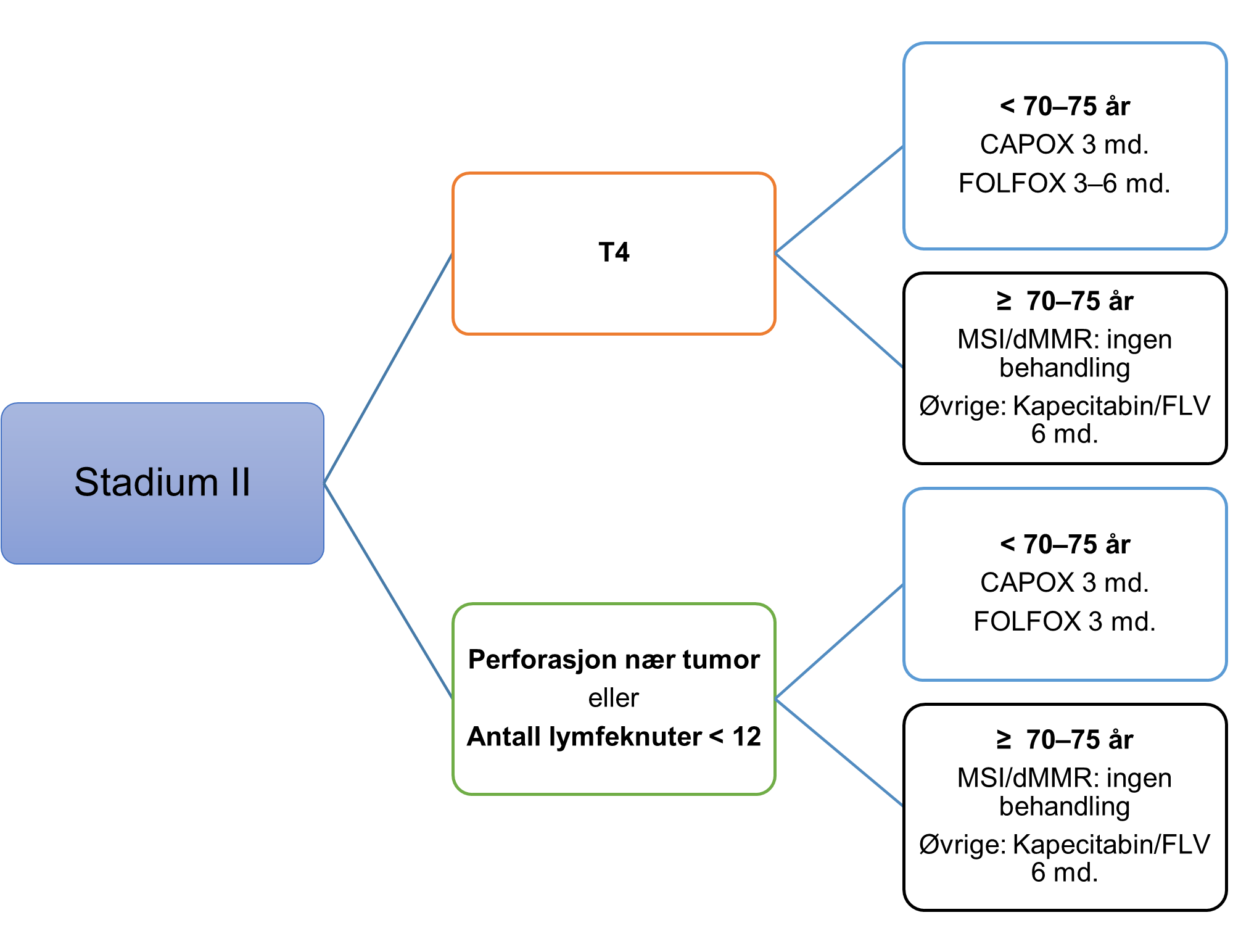
Det finnes lite evidens for nytte av adjuvant behandling ved stadium II da de fleste behandlingsanbefalinger er basert på subgruppeanalyser av studier for stadium II-III. Det ser imidlertid ut til at disse pasientene har god prognose uten nytte av adjuvant kjemoterapi dersom ingen risikofaktorer er til stede. Ved påvisning av risikofaktorer er derimot sannsynlighet for residiv betydelig økt og disse pasientene skal vurderes for adjuvant behandling. I Norge er disse faktorene definert som høyest risiko: tumornær perforasjon, pT4 eller få undersøkte lymfeknuter (≤12) (Edler et al., 2007; Kim et al., 2015; Zhang et al., 2016). Det er vist god effekt av adjuvant behandling ved T4 (Teufel et al., 2020). Det er ikke endelig avklart hvilke kriterier man ellers skal legge vekt på av andre kjente risikofaktorer som lav differensieringsgrad, karinvekst, perineural invasjon eller klinisk presentasjon med obstruksjon/perforasjon (Argilés et al., 2020) for å tilby adjuvant kjemoterapi. Hos pasienter med pT4-tumor anbefales CAPOX i 3-6 md. eller FOLFOX i 6 md. Ved perforasjon nær tumor (før/under operasjon) og/eller totalt antall undersøkte lymfeknuter <12 anbefales CAPOX i 3 md. eller FOLFOX i 3-6 md. Flere studier har vist at pasienter med stadium II med MSI/dMMR-tumor har bedre prognose og ikke nytte av adjuvant kjemoterapi med 5-FU alene (Ribic et al., 2003; Sargent et al., 2010; Sinicrope et al., 2011), og hos pasienter som ikke anses kandidat for oksaliplatin-basert regime bør en avstå fra adjuvant kjemoterapi.
Bivirkninger og komplikasjoner
Den vanligste dosebegrensende bivirkning ved bruk av oksaliplatin er kumulativ perifer sensorisk nevropati, som ofte utløses eller forverres av kulde. Klinisk relevant nevrotoksisitet bør føre til avbrudd i oksaliplatinbehandlingen, eventuelt dosejustering. Nevropati bedres som oftest med tiden, men kan gi livsvarige plager. I en randomisert studie fant man vedvarende nevropati i mer enn to år hos >10 % av pasientene hvor de alvorligste (grad III-IV) forekomr hos <1 % etter 1–2 år (Land et al., 2007). I en populasjonsbasert finsk studie ble det rapportert nevropati hos 69 % (grad I/II/III/IV hos 36/24/8/1%) ved median 4,2 år etter endt adjuvant behandling (Soveri et al., 2019). Andre bivirkninger er allergiske reaksjoner, kuldeintoleranse, larynxspasme, diare og hånd-fot syndrom.
Neoadjuvant behandling
Nytten av neoadjuvant behandling er fortsatt ikke helt avklart. I en nylig studie ble pasienter med tykktarmskreft T3-4 randomisert til 6 uker neoadjuvant oksaliplatinbasert kjemoterapi eller ikke, og 98 % ble operert. Etter neoadjuvant kjemoterapi ble det T og N downstaging (Morton et al., 2023). I NICHE studien, fikk pasienter med T3-4 eller N+ tykktarmskreft en kur med nivolumab/ipilimumab før kirurgi. Blant pasienter med dMMR hadde 19 av 20 patologisk komplett respons (Chalabi et al., 2020). Videreføring av studien (NICHE 2) med flere pasienter ble presentert på ESMO 2022 med oppsiktsvekkende god respons, men langtidsresultater foreligger ikke ennå.
Annet
Det pågår studier (ikke i Norge) for å undersøke nytten av PD-1-hemmer i kombinasjon med adjuvant kjemoterapi ved stadium III dMMR tykktarmskreft. Adjuvant behandling etter metastasebehandling omtales i kapittel om resektable metastaser (se kapittel 13).
Anbefalinger for adjuvant behandling:
- Adjuvant kjemoterapi anbefales til pasienter operert for tykktarmskreft stadium III og stadium II med risikofaktorer (evidensgrad A).
- Adjuvant kjemoterapi bør starte 4–6 uker postoperativt (evidensgrad D).
- Svar på DPYD-genotype skal foreligge før behandling med 5-FU/kapecitabin (evidensgrad B) (se kapittel Medikamentell behandlingsstrategi, avsnitt Molekylær og DPYD diagnostikk).
- For pasienter <70 år anbefales kombinasjonsbehandling med 5-FU/folinat eller kapecitabin og oksaliplatin (evidensgrad A).
- For pasienter 70–75 år anbefales vanligvis monoterapi med 5-FU/folinat eller kapecitabin i 6 md, men kombinasjonsbehandling kan vurderes basert på funksjonsnivå, allmenntilstand og komorbiditet (evidensgrad B). For pasienter over 75 år kan monoterapi 5-FU/folinat eller kapecitabin i 6 md. vurderes basert på funksjonsnivå, allmenntilstand og komorbiditet (evidensgrad D).
- Pasienter med stadium II dMMR/MSI har ikke nytte av monoterapi 5-FU (evidensnivå B).
- Ved neurotoksisitet kan oksaliplatin seponeres etter 3 md. og eventuell resterende behandling gis med 5-FU (evidensnivå B).
Anbefalinger for pasienter i stadium III aktuelle for kombinasjonsbehandling:
- Ved lavrisiko (T1-tumor eller 3N1) anbefales CAPOX i 3 md. eller FOLFOX i 3 md.
- Ved høyrisiko (T4-tumor eller N2) anbefales CAPOX 3 md. eller FOLFOX i 3–6 md (André et al., 2020b; Hamre, 2023).
Anbefalinger for pasienter i stadium II aktuelle for kombinasjonsbehandling:
Følgende karakteristika anses som risikofaktorer ved stadium II og anbefales adjuvant kjemoterapi:
- Ved pT4 anbefales CAPOX i 3 md. eller FOLFOX i 3–6 md.
- Ved perforasjon nær tumor (før/under operasjon) anbefales CAPOX i 3 md. eller FOLFOX i 3–6 md.
- Ved totalt antall undersøkte lymfeknuter <12 anbefales CAPOX i 3 md. eller FOLFOX i 3–6 md