Basert på overstående gjennomgang anbefales adjuvant systemisk behandling i tråd med figuren under og nærmere spesifikasjoner i de følgende tabellariske oversikter (kfr også spesifikasjoner/kommentarer) delt opp etter om genekspresjonstest er utført eller ikke:
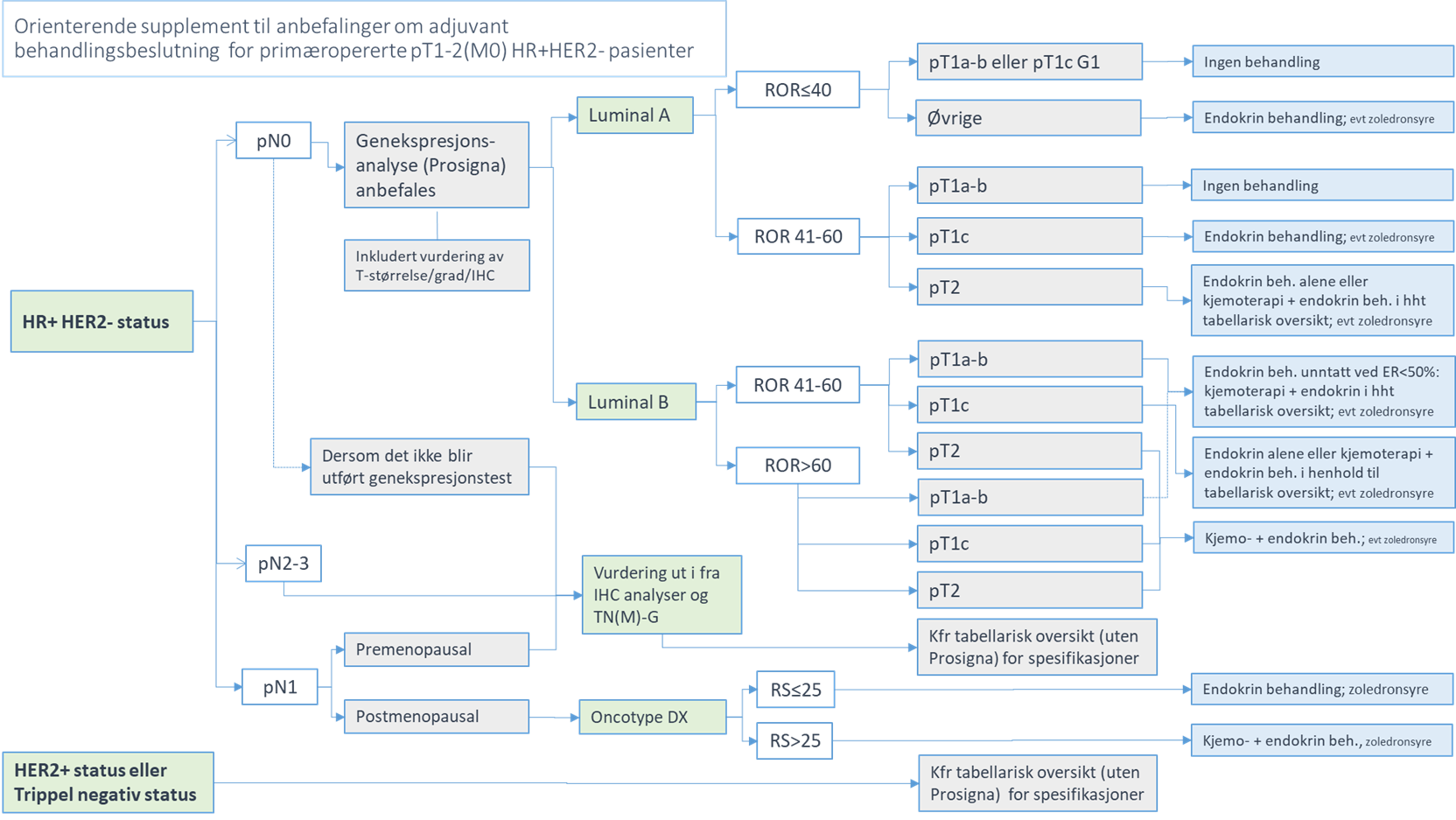
Anbefalinger for primæropererte pasienter med HR+HER2- pT1-2pN0 status eller postmenopausale pasienter med pT1-2pN1 status, hvor svar på anbefalt genekspresjonstest foreligger
Se tabell (PDF).
Anbefalinger for pasienter hvor det ikke er indikasjon for genekspresjonstest eller det ikke foreligger
Se tabell (PDF).
Fotnote/spesifikasjoner/kommentarer til anbefalingene anført i tabellene over
*Beslutningsgrunnlaget vedrørende endokrin behandling som alternativ til kjemoterapi er indirekte, og sikker kunnskap om dette alternativet for premenopausale pasienter er enda ikke tilgjengelig.
Metastaseutredning: Lymfeknute-positive pasienter som enten er HER2 positive eller trippel negative bør metastasescreenes, dersom dette ikke nevneverdig forsinker tidspunkt for behandlingsstart.
Hormonreseptorstatus: Dersom ER er negativ og PR er positiv, bør reseptorundersøkelsene gjentas for å avdekke med sikkerhet om endokrin behandling er aktuelt. PgR positivitet/ER negativitet er sjelden og oftest uttrykk for falsk positivitet (for PR) eller falsk negativitet (for ER).
Genekspresjonstester anbefales benyttet til å vurdere bruk av kjemoterapi for pasienter med HR+HER2- pT1-2pN0 status da slike tester gir sikrest prognostisk (og prediktiv) informasjon med lav interlaboratorievariabilitet. Dersom Prosigna test utføres, henvises til egen oversikt over retningslinjer, hvor testsvaret er inkludert i vurderingsgrunnlaget.
Vurdering av proliferasjon og Luminale subtyper dersom genekspresjonstest ikke er utført: Ki67 proliferasjonsindeks (estimeres som % Ki67 positive celler i hot spot) kan i tillegg til histologisk grad bidra til å skille mellom Luminal A liknende og Luminal B liknende subtyper av brystkreft (ER positive subtyper) dersom Ki67 er <10% eller >35%. Ki67 verdier mellom 10% og 35% bør ikke benyttes for vurdering av grunnlag for kjemoterapi.
Endokrin behandling. Det henvises til tekstlige anbefalinger i Handlingsprogrammet.
Calcium/VitD (1000 mg/800 IE daglig) skal i utgangspunktet gis til alle som står på AI (for eksempel Calcigran forte tyggetabletter).
Bentetthetsundersøkelser ved bruk av AI eller unge kvinner som benytter goserelin: Dersom ikke zoledronsyre benyttes som adjuvant behandling, bør det gjøres bentetthetsmålinger ved oppstart, etter 1 år og deretter hvert 2. år inntil avslutning av AI.
Zoledronsyre: Zoledronsyre gis i.v. i dosering 4 mg hver 3. måned i 2 år eller hver 6. måned i 5 år ved avdeling som vanligvis gir kjemoterapi. Behandlingslengde 5 år. Behandlingen er kun aktuell for pasienter med postmenopausal status (naturlig eller indusert) som skal gjennomføre systemisk adjuvant behandling. Tannstatus bør vurderes før oppstart av behandlingen.
Ikke-hormonell behandling. EC90 (epirubicin 90 mg/m2 + cyklofosfamid 600 mg/m2) gis hver 3. uke. TC i form av docetaxel 75 mg/m2 + cyklofosfamid 600 mg/m2 gis også hver 3. uke. Det gis G-CSF som primærprofylakse mot febrile neutropenier. Paklitaxel 80mg/m2 hver uke kan benyttes som alternativ til docetaxel hver 3. uke i TC regimet. I så fall gis ikke G-CSF som primærprofylakse. Ved indikasjon for taxan i sekvens med EC90: Docetaxel 100 mg/m2 hver tredje uke x 4 eller paclitaxel 80mg/m2 hver uke x 12. Ved bruk av docetaxel gis G-CSF som primærprofylakse mot febrile neutropenier. Ved HER2 positiv status og indikasjon for kjemoterapi: Trastuzumab eller trastuzumab+pertuzumab infusjon hver 3. uke i 1 år med oppstart samtidig med taxanbehandlingen. Gjør LVEF måling før oppstart av EC90, før oppstart av anti-HER2 behandling, deretter hver 3. mnd til avsluttet behandling. Følg egen algoritme for vurdering av LVEF i forhold til anti-HER2-behandlingen. For alternative kjemoterapiregimer, konferer tekst.
Alder og bruk av kjemoterapi og/eller zoledronsyre: Ved indikasjon, bør i utgangspunktet den skisserte adjuvante kjemoterapi og/eller zoledronsyrebehandling gis opp til minimum 75 års alder, men det anbefales ikke å benytte høy alder alene som grunn for å utelate bruk av kjemoterapi/zoledronsyre. Ved alder >70–75 år må behandling vurderes nøye i forhold til komorbiditet og leveutsikter – og individuell tilpasning kan være nødvendig.
Strålebehandling (for pasienter som ikke gjennomgår neoadjvuant behandling): Aktuelt hvis 1) operert brystbevarende, 2) ikke fri margin etter ablatio, eller 3) pN1(>2 mm)-pN3.
Ved indikasjon for kjemoterapi og planlagt 12 ukers behandlingsperiode, henvis til stråleterapi i forbindelse med eller 3 uker etter oppstart av behandlingen. Dersom det er planlagt 18-24 ukers behandlingsperiode, henvis til stråleterapi midtveis i behandlingen. Dersom det ikke er indikasjon for kjemoterapi, henvis til stråleterapi umiddelbart.
Veiledende behandlingsbeslutning ved bruk av Prosigna ved pT1pN1(mi)
Hovedgruppe | pT pN status | Prosignatest* | Generell terapi-anbefaling** | Grunnlag for eventuell vurdering av annet terapi-valg (eskalering eller de-ekskalering) |
|---|---|---|---|---|
HR +
HER2- | pT1pN1(mi) | Luminal A ROR score 0-40 | Endokrin behandling Zoledronsyre ved postmenopausal status | Dersom ER ekspresjonen er lav, vurder grunnlag for bruk av E C90 x 4 eller TC x 4 → endokrin behandling |
pT1pN1(mi) |
Luminal A** ROR score 41-60 | Premenopausal: E C 90 x 4 eller TC x 4 etterfulgt av endokring behandling. Endokrin behandling som inkluderer goserelin kan vurderes som alternativ til kjemoterapi.*** Postmenopausal: Endokrin behandling Zoledronsyre ved postmenopausal status |
| |
pT1pN1(mi) | Luminal B** ROR score 41-60
| ER ≥50%: E C 90 x 4 eller TC x 4 → endokrin behandling ER < 50%: E C 90 x 4 → taxan → endokring behandling Zoledronsyre ved postmenopausal status | Ved ER ≥50%: Endokring behandling kan vurderes ved kombinasjonen av histologisk grad 1-2 og lav absolutt ROR score | |
pT1pN1(mi) | Luminal B** ROR score >60
| E C 90 x 4 → taxan → endokrin behandling Zoledronsyre ved postmenopausal status | TC x 6 er et akseptabelt alternativ til E C90 x 4 → taxan spesielt ved cardiale risikofaktorer som gjør at man vil unngå antra cycliner. |
* I noen få tilfeller vil molekylær subtype for HR+HER2- svulster være «Basal»- eller «HER2-enriched», adjuvant behandling vil da følge ROR score og Luminal B subtype.
** Alder og absolutt ER ekspresjonsnivå kan gi grunnlag for individuell vurdering av behandlingsvalg. Dersom absolutt ROR score er meget nær cut-off verdier
for å skifte subgruppe kan det gi grunnlag for individuell vurdering av behandlingsvalg.
*** Beslutningsgrunnlaget vedrørende endokrin behandling som alternativ til kjemoterapi er indirekte, og sikker kunnskap om dette alternative for premenopausale pasienter er enda ikke tilgjengelig.