Omtrent 10–15 % av pasienter med muskelinfiltrerende blærekreft har påvisbare metastaser ved diagnosetidspunkt (Rosenberg et al., 2005). Videre vil omtrent halvparten av cystektomerte pasienter få tilbakefall av sykdommen, ca. 30 % som lokale residiv i bekkenet, øvrige med fjernmetastaser. Median overlevelse uten kjemoterapi er samlet 3–6 måneder for pasienter med metastaser (Sternberg et al., 2003b).
Førstelinjebehandling
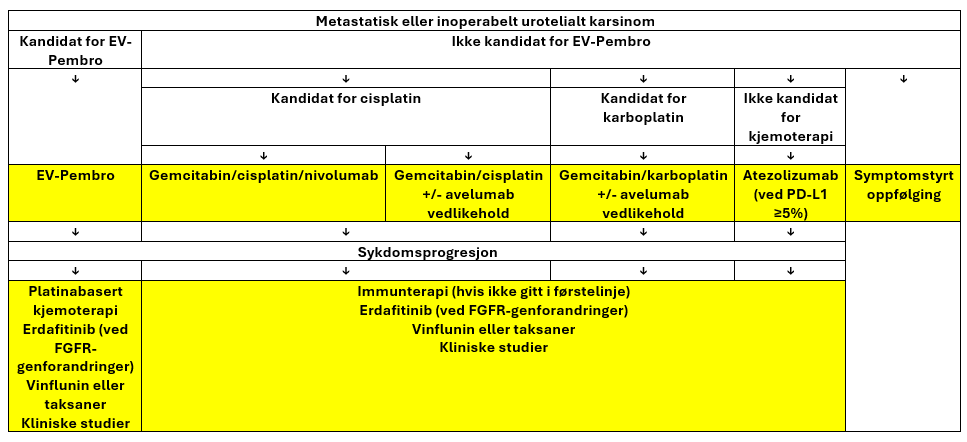
Dette flytskjemaet viser behandlingsmulighetene ved metastatisk eller inoperabelt urotelialt karsinom. Platinabasert kjemoterapi har i tiår år vært standard førstelinjebehandling for disse pasientene, men i senere år har kombinasjonen av kjemo- og immunterapi kommet til, og immunterapi alene kan også være aktuelt. Kombinasjonen nfortumabvedotin + pembrolizumab (EV-Pembro) ble godkjent som førstelinjebehandling i Norge sommeren 2025 og har tatt over som standard førstelinjebehandling hos pasienter som er kandidater for denne kombinasjonen. Erdafitinib ble samtidig innført som et alternativ i senere linjer for pasienter med spesifikke FGFR3-genforandringer.
Behandling i førstelinje
Enfortumabvedotin - pembrolizumab
Enfortumabvedotin (EV) er et antistoff-legemiddelkonjugat (ADC) bestående av et humant monoklonalt antistoff rettet mot nektin-4, et overflateprotein som er høyt uttrykt ved urotelialt karsinom, konjugert til MMAE (monometylauristatin E), som har cytotoksisk effekt på mikrotubulinettverket i cellen (Challita-Eid et al., 2016).
Kombinasjonen EV-Pembro ga omtrent en dobling av totaloverlevelse (OS) og progresjonsfri overlevelse (PFS) sammenlignet med platinabasert kjemoterapi i en større randomisert studie av pasienter med metastatisk eller inoperabelt urotelialt karsinom (Powles et al., 2025), se tabell under.
EV-Pembro gir andre bivirkninger enn tradisjonell kjemoterapi, og man må være spesielt oppmerksom på hudreaksjoner, perifer nevropati og hyperglykemi. EV-Pembro ble godkjent som førstelinjebehandling i Norge sommeren 2025 for pasienter som også er kvalifisert for platinabasert kjemoterapi. Det kreves ECOG 0-2 og akseptabel nyrefunksjon, men også godt regulert blodsukker og ingen kontraindikasjoner mot immunterapi.
Kjemo-immunterapi
Cisplatinbasert kjemoterapi inntil nylig vært den mest effektive systemiske behandlingen for urotelialt karsinom (Stenzl et al., 2011a). For at cisplatinbaserte regimer skal kunne anvendes, bør pasientene ha adekvat nyrefunksjon og god allmenntilstand med ECOG-status ≤ 1. Videre bør hørsel, eventuell nevropati og hjertefunksjon tas med i vurderingen. Omtrent 50 % av pasientene er uaktuelle for cisplatinbasert kjemoterapi grunnet nedsatt nyrefunksjon, nedsatt allmenntilstand eller annen organsykdom som f.eks. hjertesvikt. Ved kontraindikasjoner mot cisplatinbasert kjemoterapi er kombinasjonen gemcitabin/karboplatin best dokumentert (De Santis et al., 2012).
Kjemoterapi kombineres med immunterapi hos aktuelle pasienter. Gemcitabin/cisplatin kombinert med nivolumab ble innført høsten 2024 etter positive resultater i CheckMate 901-studien (inntil 6 kurer gemitabin/cisplatin/nivolumab etterfulgt av nivolumab alene i inntil to år) (van der Heijden et al., 2023). Et annet aktuelt regime er platinumbasert kjemoterapi alene (4-6 kurer gemcitabin/cisplatin eller gemcitabin/karboplatin) etterfulgt av vedlikeholdsbehandling med avelumab, som ble innført høsten 2021 som følge av JAVELIN Bladder 100-studien (Powles et al., 2020). JAVELIN-resultatene ble publisert mens CheckMate-studien fortsatt pågikk, og andelen som fikk immunterapi før progresjon i kontrollarmen i CheckMate-studien var bare 14,5 %. Resultatene fra disse studiene kan ikke direkte sammenlignes med hverandre.
Ved kontraindikasjoner mot immunterapi er platinabasert kjemoterapi alene aktuell førstelinjebehandling. Gemcitabin/cisplatin har sammenlignbar effekt med MVAC i denne settingen, men mindre toksisitet, og anses derfor som foretrukket kjemoterapiregime i metastatisk setting (von der Maase et al., 2000). Ved kontraindikasjoner mot cisplatin er gemcitabin/karboplatin aktuelt.
Studie | Studiearmer | Median OS (mnd.) | Median PFS (mnd.) | Responsrate (%) | Median varighet av respons (mnd.) | Komplett respons (%) | Median varighet av komplett respons (%) | Referanse |
|---|---|---|---|---|---|---|---|---|
EV-302 | Enfortumabvedotin + pembrolizumab vs. platinabasert kjemoterapi | 33,8 vs. 15,9 | 12,5 vs. 6,3 | 67,5 vs. 44,2 | 23,3 vs. 7,0 | 30,4 vs. 14,5 | NR vs. 15,2 | Powles et al. (2025) |
CheckMate 901 | Gemitabin/cisplatin + nivolumab vs. gemcitabin/cisplatin | 21,7 vs. 18,9 | 7,9 vs. 7,6 | 57,6 vs 43,1 | 9,5 vs. 7,3 | 21,7 vs. 11,8 | 37,1 vs. 13,2 | van der Heijden et al. (2023) |
JAVELIN Bladder 100 | Avelumab vedlikehold vs. BSC etter platinabasert kjemoterapi | 21,4 vs. 14,3 | 3,7 vs. 2,0 | * | * | * | * | Powles et al. (2020) |
*For JAVELIN-studien er det vanskelig å angi responsrate og -varighet i en slik forenklet tabell, da randomiseringen skjedde etter at pasienten allerede hadde fullført kjemoterapiperioden. Det angis «sykdomskontroll» hos 41,1 % av pasientene i avelumab-armen mot 27,4 % i kontrollarmen. Se tabell 2 i originalartikkelen for detaljer.
Immunterapi alene
Opptil 2/3 av pasientene med metastatisk urotelialt karsinom kan være uaktuelle for platinabasert kjemoterapi grunnet nyre- eller hjertesvikt, annen komorbidet eller nedsatt allmenntilstand. Immunterapi alene kan være aktuelt for disse pasientene. Atezolizumab ble godkjent høsten 2022 som monoterapi ved lokalavansert eller metastatisk urotelialt karsinom hos pasienter som ikke anses egnet for cisplatin, og hvor tumor har PD-L1-uttrykk ≥5 %. Dette er basert på en post hoc-analyse av pasienter i IMvigor 130-studien. I denne subgruppen fant man en median OS på 18,6 mnd. i atezolizumab-armen mot 10 mnd. i kjemoterapiarmen, men relevant pasientpopulasjon i studien er liten (under 100 pasienter) og ujevnt fordelt mellom armer, og resultatene må tolkes med forsiktighet (Bamias et al., 2024; Galsky et al., 2020).
Behanding ved progresjon
Ved progresjon på førstelinjebehandling er det aktuelt med enten platinabasert kjemoterapi eller immunterapi, dersom dette ikke er gitt i førstelinje. Både nivolumab, atezolizumab og pembrolizumab er godkjent i denne settingen. Hos pasienter med god initial respons på platinabasert kjemoterapi og med en lang progresjonsfri periode (minimum 6 måneder) kan ny behandlingssyklus med samme regime vurderes.
Ved progresjon etter immunterapi der det samtidig foreligger spesifikke FGFR3-genforandringer, er peroral behandling med FGFR-hemmeren Erdafitinib aktuelt. Slike genforandringer forekommer hos ca. 20 % av pasienter med avansert eller metastatisk urotelialt karsinom (ca. 36 % ved urotelialt karsinom i øvre urinveier). I THOR-studien ble Erdafitinib sammenlignet med kjemoterapi (docetaksel eller vinflunin), og median OS var 12,1 mnd. i Erdafitinib-armen mot 7,8 mnd. i kjemoterapiarmen (Loriot et al., 2023). Forekomsten av grad 3- eller grad 4-bivirkninger var omtrent lik i begge armer (ca. 46 %).
I en åpen randomisert fase 3-studie ble pasienter som hadde progrediert på platinabasert kjemoterapi og immunterapi randomisert til enten EV eller kjemoterapi (taksan eller vinflunin) (Powles et al., 2021). Resultatene viste en signifikant forbedret overlevelse i EV-armen (12,9 mnd. vs. 9,0 mnd.). EV i denne settingen ble i mai 2023 avslått i Nye metoder.
Dokumentasjonen for immunterapi som behandling i andre linje er oppsummert under. Dokumentasjonen for kjemoterapi i andre linje er svak. Det foreligger per i dag ingen dokumentasjon på systemisk behandling etter EV-Pembro i førstelinje, og inklusjon i studier bør vurderes hvis mulig.
Immunterapi
I en randomisert fase 3-studie (Keynote 045) ble PD-1-hemmeren pembrolizumab sammenlignet med kjemoterapi (paklitaksel, docetaksel eller vinflunin) hos 542 pasienter med avansert urotelial kreft som hadde residivert eller progrediert etter cisplatinbasert kjemoterapi (Bellmunt et al., 2017; Stenzl et al., 2011a; Stenzl et al., 2011b). Pasientene behandlet med pembrolizumab hadde signifikant økt median totaloverlevelse (10,3 vs. 7,4 mnd.; p=0.002). Den objektive responsraten var signifikant høyere for pembrolizumab (21,1 % vs. 11,4 %; p=0.001) og behandlingen ga færre bivirkninger. Nytten av pembrolizumab syntes å være uavhengig av PD-L1 utrykk på tumorceller og immunceller. Pembrolizumab anbefales som andrelinjes behandling for pasienter i god allmenntilstand (ECOG ≤ 2).
I en tilsvarende randomisert fase 3-studie (IMvigor211) ble PD-L1-hemmeren atezolizumab sammenlignet med kjemoterapi (paklitaksel, docetaksel eller vinflunin) hos 931 pasienter med avansert urotelial kreft som hadde residivert eller progrediert etter cisplatinbasert kjemoterapi (Powles et al., 2018; Stenzl et al., 2011a; Stenzl et al., 2011b). Det primære endepunktet var totaloverlevelse. Dette ble testet hierarkisk i predefinerte grupper avhengig av PD-L1-utrykk på tumorinfiltrerende immunceller, IC2/3 (≥5 % ekspresjon) etterfulgt av IC1/2/3 (1-<5 %), etterfulgt av «intention to treat»-populasjonen. I gruppen med IC2/3 (n=234) var totaloverlevelsen ikke signifikant bedre enn i kjemoterapigruppen (median 11,1 vs. 10,6 mnd.). Den objektive responsraten var 23 % for atezolizumab og 22 % for kjemoterapi, og dette utelukket formelle statistiske analyser av de etterfølgende populasjonene. Median varighet av respons var tallmessig lengre for atezolizumab enn for kjemoterapi (15,9 mnd. vs. 8,3 mnd). I «intention to treat»-populasjonen var det færre av dem som fikk atezolizumab enn av dem som fikk kjemoterapi som fikk grad 3–4-bivirkninger (20 % vs. 43 %) og som måtte avbryte behandlingen på grunn av bivirkninger (7 % vs. 18 %). Atezolizumab anbefales fremfor kjemoterapi som andrelinjes behandling til pasienter i god allmenntilstand (ECOG ≤ 2).
PD-1-hemmeren nivolumab har blitt testet i en enarmet fase 2-studie (CheckMate275) hos pasienter som tidligere har progrediert eller residivert etter platinabasert kjemoterapi (n=270) (Sharma et al., 2017). Objektiv responsrate var 19,6 % og respons ble sett for alle nivåer av PD-L1-ekspresjon på tumorcellene. Etter 7 måneders oppfølging var median totaloverlevelse 8,7 mnd. For pasienter som responderte var median responstid ikke oppnådd (7,43 mnd. – «not reached») og 77 % hadde fortsatt respons. Nivolumab anbefales som alternativ til kjemoterapi som andrelinjes behandling til pasienter i god allmenntilstand (ECOG ≤ 2). Ingen av PD-1-/PD-L1-hemmerne er sammenlignet direkte mot hverandre.
Kjemoterapi
Dokumentasjon av overlevelsesgevinst av kjemoterapi i andre linje er svak. Det foreligger bare en randomisert fase 3-studie. Vinflunin, et 3.-generasjons vinkaalkaloid, ble testet mot «best supportive care (BSC)» hos pasienter tidligere behandlet med platinabasert kjemoterapi (Bellmunt et al., 2013; Bellmunt et al., 2009). Denne studien ga en total responsrate på 8,6 % i vinflunin-armen, og ingen statistisk signifikant forskjell i totaloverlevelse versus BSC i «intention to treat»-populasjonen (n=370, 6,9 mnd. vs. 4,6 mnd., p=0,29). Imidlertid ble denne forskjellen signifikant etter eksklusjon av pasienter som ikke oppfylte inklusjonskriteriene (n=357, 6,9 mnd. vs. 4.3 mnd., p=0,04) (Bellmunt et al., 2009). Taksan som monoterapi er undersøkt i eldre, små fase 2-studier og brukt som komparator i nyere fase 3-studier, og kan vurderes som alternativ til vinflunin (Raggi et al., 2016).
Anbefalinger
- Førstelinjebehandling:
- Enfortumab Vedotin (EV) kombinert med Pembrolizumab (EV-P) er førstevalg.
- Ved kontraindikasjoner mot EV anbefales platinabasert kjemoterapi etterfulgt av avelumab vedlikehold eller kombinasjonsbehandling med gemcitabin/cisplatin/nivolumab.
- Ved kontraindikasjon mot platinabasert kjemoterapi kan monoterapi med atezolizumab vurderes ved PD-L1 ≥ 5 % i tumor.
- Ved kontraindikasjon mot immunterapi anbefales GC, evt karboplatin-kombinasjon ved nyresvikt
- Senere behandlingslinjer:
- Det anbefales å vurdere molekylærdiagnostikk, gjerne innenfor InPred, spesielt med tanke på FGFR-mutasjon/fusjon.
- Det foreligger per i dag ingen dokumentasjon på systemisk behandling etter EVP i første linje og inklusjon i studier bør vurderes hvis mulig. Vi anbefaler at aktuelle pasienter vurderes for platinabasert kjemoterapi, eventuelt erdafitinib ved påvist FGFR-mutasjon/fusjon. I senere linjer kan kjemoterapi med taksan eller vinflunin vurderes.
- Hvis platinabasert kjemoterapi og immunterapi er gitt som førstelinjes behandling anbefales erdafitinib hvis aktuelt, alternativt kjemoterapi med taksan eller vinflunin