Behandling av EOC er i Norge sentralisert, siden studier viser at behandling ved sykehus med spesialkompetanse i gynekologisk onkologi kan gi bedre langtidsoverlevelse (Giede et al., 2005; Paulsen et al., 2006; Tingulstad et al., 1999; Vernooij et al., 2007) og er kostnadseffektivt (Bristow et al., 2007).
Kirurgi
Terminologi
- Primæroperasjon: Operasjon uten forutgående kjemoterapi.
- Primær stagingoperasjon for tentativ stadium I-IIa. Operasjon for stadiebestemmelse.
- Primær debulkingoperasjon (PDS) for stadium ≥IIb.
- Intervall debulkingoperasjon (IDS): Operasjon etter som regel 3, eventuelt 2-5 kurer kjemoterapi.
- Restaging: Operasjon for stadiebestemmelse der dette ikke er utført ved primæroperasjon. Det foreligger ingen synlig resttumor.
- Palliativ operasjon: Symptomlindrende operasjon.
- Full staging-operasjon: Enten full peritoneal staging eller også med full glandelstaging.
Formål
- PDS og IDS: Målet er å oppnå null makroskopisk resttumor (Residual disease; RD=0) (Fotopoulou et al., 2021), og hvis dette ikke er mulig tilstrebes RD< 1 cm. Ved PDS er formålet med operasjon i tillegg å påvise riktig stadium. Hvis det ikke anses mulig å fjerne alt tumorvev > 1 cm, eller det kreves langvarig eller risikabel operasjon med usikkert utfall for å oppnå dette, avsluttes inngrepet. Representativ biopsi uten å risikere forsinket oppstart kjemoterapi bør tas. Tarmkirurgi skal i slike tilfeller kun vurderes ved truende ileus. Pasienten vurderes for NACT og deretter IDS.
- Staging: Utføre fullstendig staging der det er relevant mistanke om/risiko for oversette metastaser/mikrometastaser ved primærkirurgi eller ved restaging, og der dette har terapeutisk betydning.
- Palliativ operasjon: Målet er å dempe symptomer, for eksempel pga ileus, fistel eller ved stor primærtumor og/eller store omentmetastaser som er lett tilgjengelig for ekstirpasjon.
Diagnostisk laparoskopi/laparotomi ved stadium IIIC og IV kan utføres for å vurdere operabilitet ved usikkerhet om radiologiske funn. Det skal da tas biopsi for HRD testing dersom ikke dette er gjort tidligere.
Anbefalt kirurgisk prosedyre (Querleu et al., 2017)
Primæroperasjon
Stadium I – IIa
Stagingoperasjon inkluderer peritoneal staging og glandelstaging. Peritoneal staging er obligatorisk, glanderstaging avhenger av histologi.
Anbefalt kirurgisk prosedyre:
- Laparotomi med midtlinjesnitt. Ved tydelig stadium I kan laparoskopi med full staging utført av gyn. onkolog aksepteres.
- Ascites eller peritoneal skyllevæske til cytologi.
- Systematisk beskrivelse av hele bukhulen og evntuelt angivelse av PCI (peritoneal cancer index) score (Jacquet et al., 1996).
- Bilateral salpingo-oophorektomi (BSOE).
- Hysterektomi.
- Omentektomi, infrakolisk.
- Lymfadenektomi i bekkenet og para-aortalt opp til venstre nyrevene, inngår som ledd i stadieinndeling (Camara et al., 2009; Harter et al., 2017). G1 EC og ekspansiv MC FIGO st. IA: Ingen sikker indikajson for glandelstaging pga lav risiko for lymfeknutemetastasering. Nytten av lymfadenektomi ved LGSC er uklar.
- Suspekte lesjoner ekstirperes. Dersom det ikke foreligger suspekte lesjoner anbefales blindet peritoneal biopsi fra bekken, parakolisk og subdiafragmalt.
- Frysesnitt kan være aktuelt.
- Tumorruptur (bør unngås) og grad av adheranser skal registreres.
Mucinøst carcinom (Hess et al., 2004): Appendix fjernes i tillegg. Full tumorekstirpasjon har prognostisk betydning.
Usikker origo eller mistenkt pseudomyxoma peritonei: Gastrokirurg bør konsulteres, helst preoperativt. Det kan være aktuelt med HIPEC (hyperterm intraperitoneal kjemoperfusjon).
Restaging ved stadium I (Colombo et al., 2019a; González-Martín et al., 2023) og STIC (Weinberger et al., 2016; Wethington et al., 2013)
Ved antatt benign tumor, der histologien uventet er malign, henvises pasienten til gynekologisk kreftsenter for vurdering for komplett staging og kjemoterapi. Anbefalt kirurgisk prosedyre som beskrevet over kan utføres med minimal invasiv kirurgi.
Full staging-operasjon utføres etter primæroperasjon hvis det er relevant risiko for metastaser, og vurderes i forhold til tumortype, pasientens almentilstan og preferanse og eventuelt valg av videre adjuvant kjemoterapi og vedlikeholdbehandling. Peritoneal staging er obligatorisk. Lymfadenektomi kan unnlates dersom lymfeknutestatus ikke endrer pasientens videre behandling. Hos høy-risiko pasienter som anbefales adjuvant kjemoterapi må lymfadenektomi for prognostisk stadiebestemmelse vurderes opp mot potensiell morbiditet ved prosedyren (Colombo et al., 2019a). Det vises til kapittelet om medikamentell behandling og flytskjema for adjuvant behandling nedenfor.
Idet risiko for lymfeknutemetastaser er <1% ved G1 EC og ekspansiv MC (González-Martín et al., 2023; Heitz et al., 2018) anbefales ikke lymfadenektomi hos disse pasientene. Nytten av lymfadenektomi ved LGSC er uklar, og kan unnlates (González-Martín et al., 2023).
Ved MC utføres også appendektomi, men reoperasjon for appendectomi alene er ikke indisert hvis appendix er beskrevet normal.
Serøs tubart intraepitelialt karsinom (STIC) påvist: Kirurgisk prosedyre som beskrevet over bortsett fra lymfadenektomi. Premenopausale vurderes individuelt. Det er ikke vist at lymfadnektomi og/eller kjemoterapi gir bedre prognose hvis kun STIC er påvist (Wethington et al., 2013), og anbefales derfor ikke. Skyllevæske tas fordi bukhulen er vanligste sted for spredning. Histologi med SEE-FIM prosedyre (3 mm tette snitt) av tuber/ovarier (Powell et al., 2011), jmf. Kapittel 3.3 Patologi. Pasienten bør anbefales gBRCA1/2 testing.
Fertilitetsbevarende kirurgi
Fertilitetsbevarende behandling krever grundig samtale med pasienten med objektiv informasjon som inkluderer vurdering av mulighet for graviditet, behandlingsalternativ, risiko for tilbakefall og prognose. Ved fertilitetsbevarende kirurgi foretas regranskning av histologi, og endometriebiopsi anbefales på diagnosetidspunktet.
Europeiske anbefalte seleksjonskriterier for ovarial preservasjon (Morice et al., 2024)
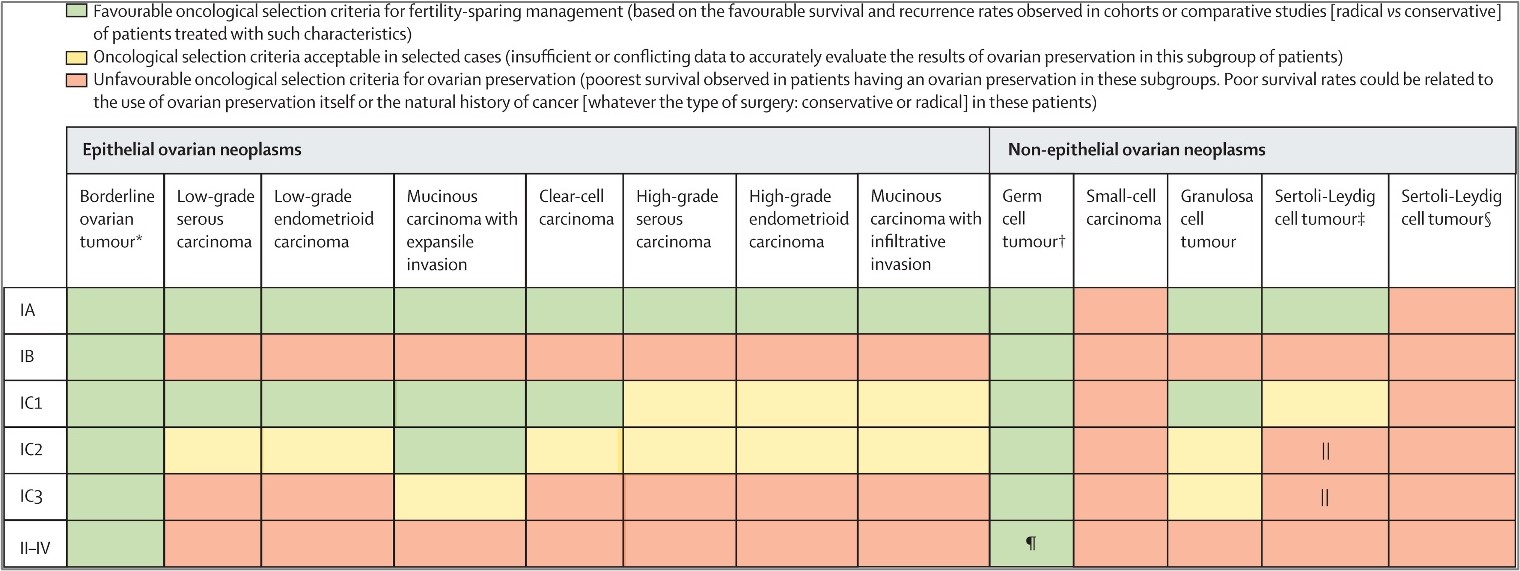
Kirurgisk prosedyre: Ensidig salpingo-oophorektomi eller tumorreseksjon uten ruptur, cytologi fra bukskyllevæske, omentektomi og eventuelt lymfeknutestaging, jmf primæroperasjon over (Morice et al., 2024).
Pasienten kan anbefales graviditet 1 år etter avsluttet behandling såsant det ikke er mistanke om residiv (Morice et al., 2024). Når pasienten ikke lenger har barneønske, bør man vurdere å fjerne gjenværende adnex/ovarium ved tumor med serøs histologi.
Stadium IIb–IV
Anbefalt kirurgisk prosedyre:
- Laparotomi med midtlinjesnitt.
- Ascites eller peritoneal skyllevæske for cytologi.
- Systematisk beskrivelse av hele bukhulen.
- Grad av adheranser, innvekst og tumorruptur registreres.
- Hysterektomi.
- Bilateral salpingo-oophorektomi.
- Omentektomi.
- Infrakolisk ved stadium II
- Parakolisk ved stadium III og IV
- Ekstirpasjon av all carcinomatose.
- Tarmreseksjon, splenektomi, diafragmastripping ved behov.
- Lymfadenektomi (Bachmann et al., 2015; Camara et al., 2009):
- Ved stadium IIB–IIIC fjernes «bulky nodes» og metastasesuspekte lymfeknuter beskrevet på CT (Harter et al., 2017; Panici et al., 2005).
- Ved stadium IV fjernes forstørrede, resektable lymfeknuter beskrevet på CT (kardiofrenisk, supraklavikulært, i lysker og axiller).
Resttumor med størrelse, lokalisasjon og limiterende årsak skal dokumenteres i operasjonsbeskrivelse. ESGO surgical score kan benyttes.
Intervall debulkingoperasjon (IDS)
Utføres vanligvis 3–4 uker etter 3. eller 4. kur etter ny vurdering på MDT møte. Ved lungeemboli kan IDS utføres etter 2. kur så sant ikke andre stoppkriterier foreligger.
Det er overlevelsesgevinst ved null resttumor, og det er også vist at kirurgi etter 3. kur kan gi overlevelsesgevinst hvis resttumor < 1 cm kan oppnås (du Bois et al., 2009). Hvis IDS utføres etter 5. kur er det kun vist overlevelses gevinst ved null resttumor (Phillips et al., 2018). Ytterligere 2 kurer må vurderes postoperativt.
Ved forventede restforandringer mellom 1 og 2 cm, foretas individuell vurdering, idet gevinsten er mindre. Derfor vil man normalt ikke utføre store, langvarige eller risikable operasjoner for å oppnå dette målet (Bristow et al., 2006; Gill et al., 2017; Kehoe et al., 2015; Kessous et al., 2017; Marchetti et al., 2017; Phillips et al., 2018; Vergote et al., 2010).
Medikamentell behandling
Støtteinformasjon for de ulike medikamentene for infusjon, der bl.a. dosering, kurintervall, antiemetika/premed, forundersøkelser, blodprøvekrav og bivrkninger inngår, finnes i CMS kurbibliotek: CMS kurbibliotek (OUS/HSØ).
Inklusjon i studier skal alltid tilstrebes.
Terminologi
Terapeutisk behandling: Medikamentell behandling som virker mot manifest sykdom. Gis postoperativt ved avansert sykdom, neoadjuvant eller hvor kun medikamentell behandling gis.
Adjuvant behandling: Tilleggsbehandling med medikamentell behandling etter operasjon hvor all detekterbar sykdom er fjernet, men hvor det gjenstår en risiko for tilbakefall på grunn av okkult sykdom.
Neoadjuvant kjemoterapi (Neoadjuvant chemotherapy, NACT): Kjemoterapi som gis før planlagt operasjon for å redusere tumormengde, optimalisere pasientens almenntillstand eller ved lungeemboli.
Stadium I
Indikasjon for adjuvant kjemoterapi ADDIN EN.CITE.DATA (González-Martín et al., 2023; Ledermann et al., 2024)
Det er vist at adjuvant platinumbasert kjemoterapi signifikant forlenger OS og PFS ved tidlig stadium EOC (Collinson et al., 2014; Lawrie et al., 2015; Trimbos et al., 2003), men at effekten avhenger av subgruppe og understadie (Collinson et al., 2014; Gouy et al., 2017; Mizuno et al., 2012; Oseledchyk et al., 2017).
Standard adjuvant behandling består av seks sykler med platinumbasert kjemoterapi. Dog mangler det evidens for optimalt kjemoterapiregime; platinum alene eller i kombinasjon med paklitaksel (Collinson et al., 2014). En randomisert fase 3 studie har ikke vist signifikant reduksjon i risiko for tilbakefall ved 6 i forhold til 3 kurer med karboplatin og paklitaksel for høyrisiko pasienter (Bell et al., 2006), og en utforskende analyse av denne studien viste at kun serøse carcinomer ser ut til å profittere på 6 kurer (Chan et al., 2010). Anbefalinger for adjuvant kjemoterapi samt retningsgivende regime og antall kurer er anført i hhv Figur 5 og Tabell 3 nedenfor, og vurderes i forhold til gjennomført kirurgi og pasientens almentilstand.
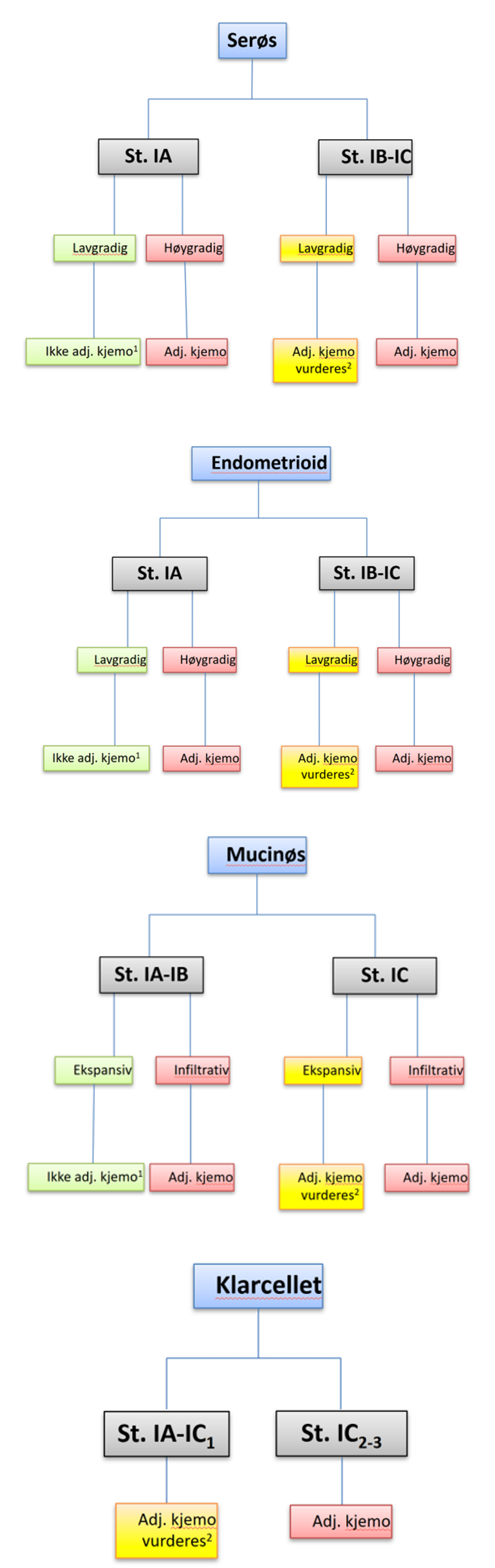
1 Forutsetter full staging
2 Kan unnlates ved full staging
Full staging: Peritoneal- og eventuelt glandelstaging.
| Serøs | 1A, lavgradig | Ingen adjuvant kjemoterapi (forutsetter full staging). |
1B, lavgradig | Adjuvant kjemoterapi (karboplatin og paklitaksel x 3 eller karboplatin singel x 6). Kan unnlates ved full staging. | |
| 1C, lavgradig | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6 eller karboplatin singel x 6). Kan unnlates ved full staging. | |
1A-C, høygradig | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6). | |
| Endometrioid | 1A, lavgradig | Ingen adjuvant kjemoterapi (forutsetter full staging). |
1B-C, lavgradig | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6 eller karboplatin singel x 6). Kan unnlates ved full staging. | |
1A-C, høygradig | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6). | |
| Mucinøs | 1A-B expansiv | Ingen adjuvant kjemoterapi (forutsetter full staging). |
1C expansiv | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6 eller karboplatin singel x 6). Kan unnlates ved full staging. | |
1A infiltrativ | Adjuvant kjemoterapi (karboplatin og paklitaksel x 3 eller karboplatin singel x 6). | |
1B-C, infiltrativ | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6) | |
| Klarcellet | 1A-1C1 | Adjuvant kjemoterapi (karboplatin og paklitaksel x 3 eller karboplatin singel x 6). Kan unnlates ved full staging. |
1C2–3: | Adjuvant kjemoterapi (karboplatin og paklitaksel x 6). |
Tabell 3: Retningsgivende kjemoterapiregime og antall kurer ved EOC stadium I ADDIN EN.CITE.DATA (González-Martín et al., 2023; Ledermann et al., 2024).
Stadium II–IV
Alle anbefales kjemoterapi og skal vurderes for vedlikeholdsbehandling. Pasientens almentilstand tas med i vurderingen.
Etter kirurgi bør behandlingen starte når pasienten er rimelig restituert. Tid fra kirurgi til oppstart kjemoterapi der det er null resttumor er en prognostisk faktor, og tilstrebes innen 3 uker (Mahner et al., 2013). Hvis preoperativ histologi foreligger, kan behandlingen startes tidligere.
NACT vurderes ved stoppkriterier for primærkirurgi. Det anbefales 3 kurer før ny CT og ny vurdering av operabilitet på MDT-møte. Det skal tas CA125 ved hver kur neoadjuvant (Bristow et al., 2006; Fotopoulou et al., 2021; Gill et al., 2017; Kehoe et al., 2015; Kessous et al., 2017; Marchetti et al., 2017; Phillips et al., 2018; Vergote et al., 2010). Postoperativt kontinueres kjemoterapi vanligvis inntil totalt 6 kurer. Hvis pasienten ikke er operabel, kontinueres kjemoterapi, totalt 6 kurer.
Kjemoterapi
Anbefalt regime er kombinasjonsbehandling med karboplatin (AUC=5) og paklitaksel (175 mg/m2) i.v., hver 3. uke, 6 kurer (Bookman, 2010; Ozols et al., 2003; Stuart et al., 2011).
Ca 20 % av pasienter med EOC har manglende respons på førstelinjebehandling, får tilbakefall få uker etter eller progredierer innen 6 mndr eller siste platinumbaserte kjemoterapi (Monk et al., 2016).
Bivirkninger/spesielle forhold:
- Kontraindikasjon mot paklitaksel; nevropati eller hypersensitivitet: Ved funksjonsnedsettende/svært plagsom nevropati (persisterende CTCAE ≥ grad 2 nevropati), høy risiko for neuropati eller hypersensitivitet byttes paklitaksel ut med docetaksel (Vasey et al., 2001).
- Kontraindikasjon mot taksaner (paklitaksel og docetaksel); nevropati eller hypersensitivitet: Taxaner kan erstattes med pegylert liposomalt doksorubicin (PLD) (Pignata et al., 2011), alternativt gemcitabin.
- Kontraindikasjon mot karboplatin
- Hypersensitivitet: Cisplatin i hypersensitivitetsregime kan forsøkes unntatt ved alvorlig anafylaksi.
- Trombocytopeni: Cisplatin kan erstatte karboplatin.Kontraindikasjon mot platinum (karboplatin og cisplatin): Trabektedin og PLD kan brukes.
- Redusert almenntillstand eller høy alder: Enkeltstoffbehandling med karboplatin (AUC 5 eller 4) kan være aktuelt (von Gruenigen et al., 2017). Ukentlig behandling med lav dose paklitaksel (60 mg/m2) og karboplatin (AUC 2) kan vurderes da det er vist bedre livskvalitet hos skrøpelige pasienter ved dette regimet (Pignata et al., 2014).
- Nyresvikt:
- Karboplatin. Ved estimert GFR <40ml/min skal det gjøres nukleærmedisinsk GFR undersøkelse (Oguri et al., 2015), og denne verdien brukes ved beregning av karboplatindosen. Svært lave GFR-verdier kan være usikre, og pasienten skal følges med blodprøver (minimum trombocytter og kreatinin). Eventuelt kontroll av målt GFR under behandling. Det er i utgangspunktet ingen nedre GFR-grense for bruk av karboplatin (Ashley et al., 2019). Avdeling for gynekologisk kreft ved DNR kan konfereres ved alvorlig eller dialysekrevende nyresvikt. Ved behov konfereres nefrolog.
- Cisplatin gis vanligvis ikke ved GFR≤50 ml/min, og skal ikke gis ved GFR<40 ml/min.
- Mucinøse karcinomer: I Norge har flere sentre i flere år hatt tradisjon for å behandle etter koloncancer regime (Gore et al., 2015; Hess et al., 2004; Shi et al., 2017). To studier, en fase II og en retrospektiv, har ikke funnet forskjell i prognose ved bruk av EOC- vs coloncancer- regime (Gore et al., 2019; Schlappe et al., 2019), mens en retrospektiv studie fant forbedret OS ved koloncancerregime (Kurnit et al., 2019). Det er altså uavklart hvilket av de to regimene som er å foretrekke (Kurnit et al., 2022). Det er enighet om at behandling med karboplatin og paklitaksel anbefales primært (Ledermann et al., 2024). Tillegg av bevazicumab kan vurderes (Gore et al., 2015; Perren, 2016). Ved manglende effekt bør platinum-fri behandling som ved koloncancer vurderes. Pasienten bør vurderes for utvidet molekylærtesting og vurdes tverrfaglig.
- Lavgradige serøse, klarcellede og mucinøse karcinomer har lavere responsrate (Goff et al., 1996; Grabowski et al., 2016; Hess et al., 2004).
- Ved kronisk eller gjennomgått Hepatitt B infeksjon: Pasienten skal monitoreres med HBV DNA og ALAT hver 3. mnd og i 12 mnd etter avsluttet immunosuppresiv behandling. Ved stigning konferer infeskjonsmedisiner mht vurdering av behandling med Entekavir tbl 0.5 mg x 1 (Reikvam et al., 2024).
Vedlikeholdsbehandling
Anbefalt vedlikeholdsbehandling ved høygradig avansert (st. III-IV) primær platinum-sensitiv EOC (Nasjonalt konsensusmøte et al., 2023) fremgår i diagrammer nedenfor.
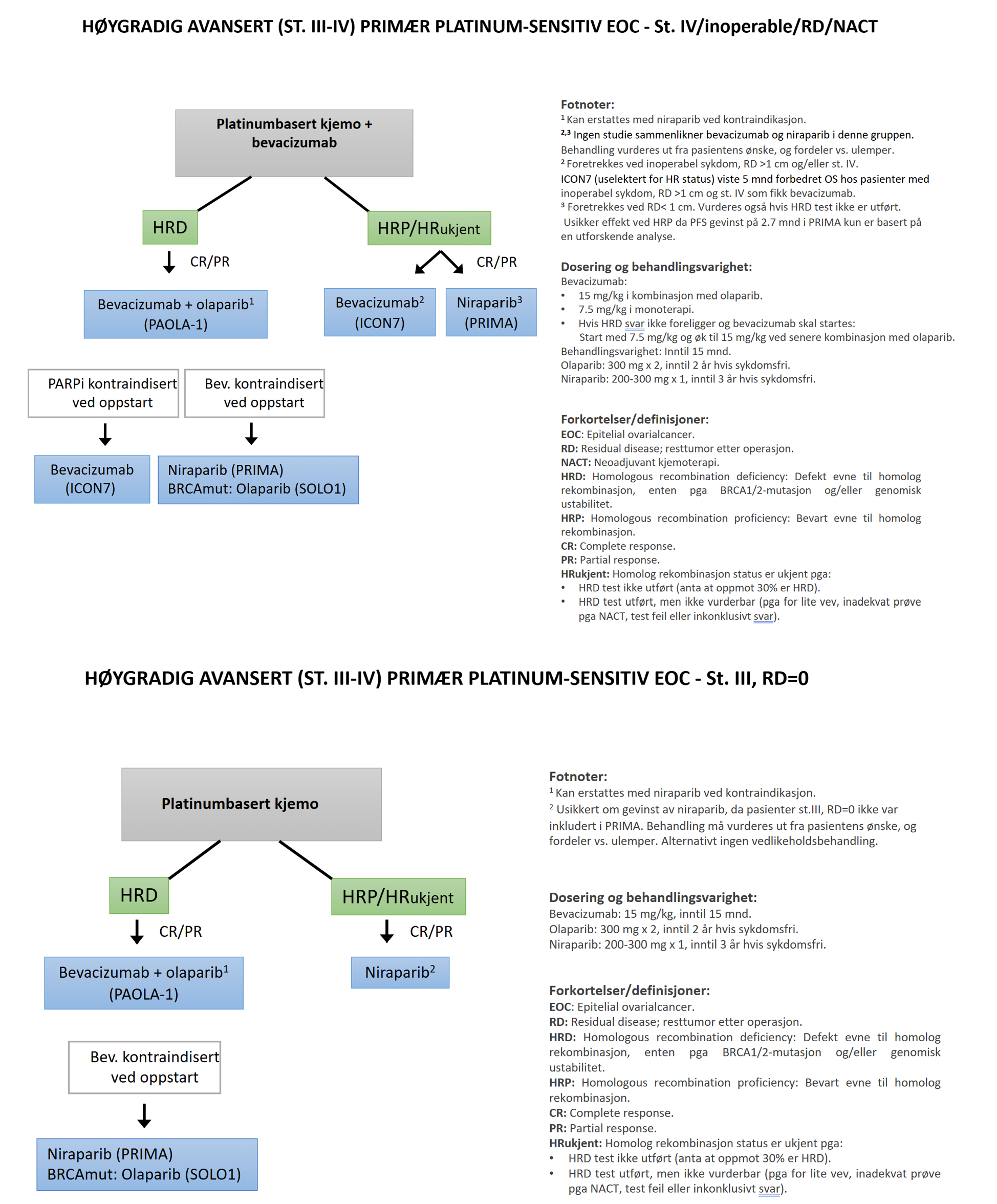
Flytskjema oppdateres i løpet av våren 2026.
VEGF-hemmer: Bevacizumab
To prospektive, randomiserte studier, GOG-218 (Burger et al., 2011) og ICON7 (Perren et al., 2011) har vist at tillegg av bevacizumab til karboplaitn og paklitaksel og deretter vedlikeholdsbehandling med bevacizumab gir signifikant økning i PFS, men ikke OS. En post-hoc subgruppeanalyse av ICON7-studien viste imidlertid økt OS for pasienter med dårligst prognose, «høyrisikogruppen»; inoperable, stadium IV eller stadium III med resttumor >1 cm etter primær operasjon. Beslutningsforum i Nye metoder har på bakgrunn av dette godkjent bruk av bevacizumab 7.5 mg/kg hver 3. uke til denne høyrisikogruppen. I tillegg ble det på NFGO styremøte i 2018 besluttet at også pasienter som har fått NACT og IDS skal inngå i «høyrisikogruppen».
Dersom pasienten skal vurderes for IDS etter 2-3 kurer kan oppstart med bevacizumab avventes til dette, idet potensiell nytte er omdiskutert (Garcia Garcia et al., 2019; Rouzier et al., 2017). Tillegg av bevacizumab til NACT kan vurderes ved store mengder ascites/pleuravæske. Bevacizumab skal ikke gis ved kjemoterapikuren rett før og rett etter kirurgi. Pasienter som ikke skal opereres kan får bevacizumab ved alle kjemoterapikurene. Bevacizumab gis uavhengig av histologi.
Anbefalt dosering og behandlingslengde fremgår i flytdiagrammene over.
Bevacizumab i kombinasjon med olaparib er indisert ved HRD-postive svulster, som det fremgår av flytskjemaet over.
PARP-hemmer
Flere randomiserte fase 3- studier med PARP-hemmer som vedlikeholdsbehandling har vist forbedret overlevelse. På bakgrunn av SOLO1- (Moore et al., 2018), PAOLA-1- (Ray-Coquard et al., 2019), og PRIMA- (González-Martín et al., 2019) og ATHENA-MONO (Kristeleit et al 2025) studiene og metodevuderinger av DMP har Nye metoder innført olaparib til bruk ved BRCA1/2 mutert sykdom (SOLO1) og, olaparib kombinert medog bevacizuamb til HRD- postive svulster (PAOLA-1). Niraparib og rucaparib er innført i Nye metoder godkjent ved fullstendig eller partiell respons på førstelinjebehandling med platinabasert kjemoterapi. PARP-hemmere er dermed i primærbehandling innført som vedlikeholdsbehandling ved FIGO stadium III-IV, høygradig EOC som har respondert (fullstendig eller delvis) på platinumbasert kjemoterapi, eller som ikke har tegn til gjenværende kreftsykdom ved avslutning av kjemoterapien.
Vedlikeholdsbehandling med niraparib eller rucaparib er et alternativ ved toksisitet eller dersom det foreligger HRP (HRD-negativ) sykdom eller ukjent HR-status. Effekten av vedlikeholdsbehandlingen er usikker hos pasienter med FIGO stadium III sykdom uten restsykdom u, da denne pasientgruppen ikke var inkludert i PRIMA- studien. ATHENA-MONO rapporterer moderat men klinisk relevant effekt i denne gruppen. For pasienter med HRP-sykdom og FIGO stadium III med resttumor eller stadium IV er effekten også usikkert, da gevinsten i PFS på 2.7 mnd i PRIMA studien er basert på en utforskende analyse. I ATHENA-MONO ble det rapportert en PFS på 12 mnd i rucaparib-armen mot 9 mnd i placeboarmen. I tillegg er det ikke funnet OS gevinst ved vedlikeholdsbehandling med niraparib i PRIMA studien (Monk et al., 2024). På bakgrunn av det overstående bør vedlikeholdsbehandling med niraparib diskuteres nøye med pasienter som har HRP sykdom.
Behandlingslengde: Olaparib inntil 2 år og niraparib inntil 3 år, men det er en åpning for at behandlingen kan kontinueres ved gjenværende sykdom. For rucaparib er behandlingslengden 2 år. Sykehusinnkjøp har ikke innført noen rangering av PARP-hemmerne i 1 linje.
Endokrin behandling
LGSC responderer generelt dårlig på kjemoterapi. De fleste LGSC har høyt uttrykk av østrogen- og progesteron-reseptorer, og positiv østrogenreseptor-status i tumor kan være en prediktor for respons av endokrin behandling (Colombo et al., 2019b), men effekt er også vist hos ved østrogenreseptor-negativ tumor. En retrospektiv studie har vist at pasienter med LGSC stadium II-IV har forbedret PFS ved endokrin vedlikeholdsbehandling etter avsluttet 1. linje-behandling (Gershenson et al., 2017). Endokrin behandling, for eksempel med aromatasehemmer, bør derfor vurderes hos disse pasientene, i utgangspunktet til progresjon. I søknad til HELFO bør det refereres til overstående artikkel som begrunnelse for refusjon. Det anbefales samtidig behandling med kasium og D-vitamin (Calcigran Forte 1000 mg/800IE x 1) for å motvirke osteoporose. Bentetthetsmåling anbefales før/ved oppstart, deretter etter ett år og deretter hvert 2. år, vurderes etter leveutsikt.
Endokrin vedlikeholdsbehandling ved primær stadium II-IV LGSC undersøkes nå i en prospektiv randomisert klinisk studie (Fader, 2019-2028; Fader et al., 2021).