Generell vurdering av resektabilitet
Kirurgi er eneste potensielt kurative behandling. Overlevelse avhenger primært av R-status, vaskulær invasjon og lymfeknutestatus. Reseksjon er beheftet med signifikant morbiditet (og for perihilære svulster også med signifikant mortalitet) og er kun aktuelt for pasienter i god allmenntilstand (WHO-ECOG status 0/1). I korthet består vurderingen av å avklare om pasienten er operabel, om tumor er resektabel, og å utelukke maligne ikke-regionale lymfeknuter eller andre metastaser. Ikke-maligne differensialdiagnoser må alltid vurderes. Hvis alt dette er tilfredsstillende kan pasienten eksploreres.
Maligne lymfeknuter utenfor leverligamentet vil i hovedsak utelukke reseksjon (unntatt for distale svulster) da prognosen er som ved metastasert sykdom (Kelly et al., 2014; Rassam et al., 2018), selv om noen av disse formelt vil kalles «regionale» etter UICC versjon 8. Hvis man skal resecere pasienter i situasjoner med patologi i formelt regionale lymfeknuter utenfor leverhilus bør inngrepet ha lav risiko da gevinsten er svært usikker. Selv N1-sykdom har stor innvirkning på overlevelse for intrahepatiske og perihilære kolangiocarcinomer, og for galleblærekreft og må med i vurderingen av mulig gevinst.
For distale kolangiocarcinomer vil i praksis alle lymfeknuter til høyre for arteria mesenterica superior være regionale og ikke utelukke reseksjon (mens aortocavale/periaortale vil regnes som M+).
Anbefaling:
- Reseksjon er kun aktuelt for pasienter i god allmenntilstand (WHO-ECOG 0/1).
Generelt om nytten av systematisk lymfadenektomi
Omtrent 40 % av pasientene med kolangiocarcinom har regional sykdom (N+) (Larsen, 2021; Liang et al., 2021). Prognosen er distinkt dårligere ved N+ status sammenliknet med N0 (Groot Koerkamp et al., 2015; Guglielmi et al., 2013; Liang et al., 2021; Morine et al., 2015). Det er ikke dokumentert om lymfadenektomi ved radikal kirurgi for kolangiocarcinom bare bedrer stadieinndeling eller om det også påvirker langtidsoverlevelse (Guglielmi et al., 2013). En nylig metaanalyse for intrahepatiske kolangiocarcinomer konkluderte med det samme (Zhou et al., 2019). Det finnes ingen RCT som kan belyse spørsmålet.
For lymfeknute-positiv sykdom rapporteres ofte et skille i langtidsoverlevelse mellom få (én eller to), eller flere lymfeknuter involvert (Liang et al., 2021; Suzuki et al., 2019). Andre peker på lymfeknuteratio, dvs. brøken med antall metastatiske lymfeknuter dividert på antall lymfeknuter ekstirpert, med en rate på 0.15–0.2 som prognostisk vannskille (Di Martino et al., 2022; Giuliante et al., 2016). Uansett rapporteres langtidsoverlevelse på opptil 10–30 % selv ved N+-sykdom, og best for de distale kolangiocarcinomene (Guglielmi et al., 2013; Morine et al., 2015; Suzuki et al., 2019). Formell lymfadenektomi er økende brukt både i vestlige og asiatiske land (Zhang et al., 2018), og selv om det er omdiskutert, må det anses som en integrert del av radikal kirurgi ved kolangiocarcinom, uansett lokalisasjon. Omfanget er spesifisert for den enkelte tumorentitet i respektive avsnitt.
UICC-manualen angir at disseksjonen ofte vil gi/bør gi minst 6 lymfeknuter ved reseksjon for intrahepatiske svulster og galleblærekreft, og 12–15 ved perihilære og distale svulster, men litteraturen peker på 6 lymfeknuter som tilstrekkelig. "Fangst" utover dette synes ikke å påvirke prognosen, men kan bidra til bedre staging (Giuliante et al., 2016; Liang et al., 2021).
Anbefaling:
- Systematisk lymfadenektomi anbefales for alle reseksjoner.
Om avlastende stenting av galleveier ved perihilære/distale kolangiocarcinomer
Som angitt over skal det ikke gjøres noen instrumentering på disse pasientene før det er konferert med senter som gjør lever- pankreas- og gallegangskirurgi (HPB-senter). Det bør uansett kun anlegges stent ved manifest kolangitt, eller som forberedelse til reseksjon eller kjemoterapi. Ikterus alene er ikke indikasjon for stenting. Pga. stentinduserte artefakter bør adekvat CT/MR/MRCP sikres før stenting. ERC og perkutant transhepatisk gallegangsdren (PTBD) har begge styrker og svakheter, og valget mellom modalitetene må individualiseres og baseres på obstruksjonsnivå, sykdomsutbredelse og lokale ressurser. Dette er pasientgrupper med spesielt høy risiko for infeksiøse komplikasjoner.
Ved resektabel eller potensielt resektabel sykdom
Der avlastning av perihilære eller intrahepatiske kolangiocarcinomer må gjøres bør dette i utgangspunktet bare omfatte fremtidig leverrest. Leversegmenter som planlegges resecert bør fortrinnsvis ikke kanyleres eller kontrastfremstilles. For distale (intrapankreatiske) kolangiocarcinomer bør stent unngås.
Der det planlegges kjemoterapi må galledrenasje sikres (bilirubinverdi forslagsvis under tre ganger øvre normalområde, evt. konferer med onkolog).
Ved ikke-resektabel sykdom
Noen pasienter vil trenge stent for å avlaste kolangitt, kløe eller for oppstart palliativ kjemoterapi. Perkutant transhepatisk galledren (PTBD) og retrograd stenting ved ERC har tradisjonelt vært ansett likeverdige for avlastning av fremtidig leverrest (FLR) forårsaket av perihilær eller hilusnær tumor (Hameed et al., 2016). En ny systematisk review konkluderer med noe mindre komplikasjoner hos pasienter som dreneres perkutant, transhepatisk (Van Eecke et al., 2022). Intrahepatiske svulster vil oftest stentes perkutant, mens helt distale og periampullære oftest stentes lettest med ERC. I en nederlandsk protokoll testes en ny teknikk («orphan stent») der en ved perkutan tilgang anbringer stent gjennom tumorbærende gallegang uten at papillen passeres og uten at det etterlates en ekstern komponent. OUS har REK-godkjenning for å inkludere pasienter i en slik kohortstudie.
Anbefaling:
- Avdeling med lever- og pankreaskirurgisk kompetanse skal ha vurdert pasienten før det gjøres noen instrumentering i galleveiene.
Volumekspanderende tiltak og preoperativ drenasje
Pasienter med svulster som affiserer hilus og medfører behov for leverreseksjoner med estimert restvolum på under 30 %, må gjennomgå preoperative volumekspanderende tiltak som portveneembolisering (PVE) (Rassam et al., 2018). Dobbeltveneembolisering (DVE) er også et alternativ. Obstruerte galleganger i fremtidig leverrest (FLR), bør avlastes før det gjøres volumekspanderende tiltak. Den leverdelen som skal reseceres dreneres ikke. Ved kjent global leversykdom (NAFLD, steatose, fibrose osv.) bør restvolumet være minst 40 % (Esnaola et al., 2016), og sannsynligvis enda høyere. Tilstrekkelig avlastning vurderes ved normalisering av bilirubin med stent kun i FLR. Hvis det er stent også i kontralaterale lever (hvilket bør unngås), kan ikke normalisering av bilirubin alene brukes som indikasjon på funksjon i FLR. I slike tilfeller bør galleveienes kaliber i FLR være helt normalisert og volumkravet økes (Wiggers et al., 2016). Ved FLR i intervallet 30–50 % er det sannsynligvis ikke indisert å gjøre volumekspanderende tiltak såfremt man er sikker på at FLR er adekvat drenert og har kommet seg. Ved FLR > 50 % er det ikke indisert med avlastning av FLR selv ved sterkt forhøyet bilirubin (Wiggers et al., 2016).
Kirurgi ved intrahepatiske kolangiocarcinomer
Anslagsvis kan én av fem pasienter opereres (Olthof et al., 2023; Valle et al., 2021). Vurderingen er i hovedsak som ved annen leverreseksjon for malign tumor. Restleverens størrelse og funksjon vurderes. Ved tumor som vokser ned mot hilus, kan reseksjon av ekstrahepatiske galleveier være nødvendig. Preoperativ kjemoterapi (down-staging) bør vurderes ved lokalt avansert intrahepatisk kolangiocarcinom (kontakt med pedikkel eller levervene i gjenstående leverrest), og ved N1-sykdom og/eller multifokalitet (Le Roy et al., 2018).
Kirurgisk reseksjon av intrahepatiske kolangiocarciomer var assosiert med en 90-dagers postoperativ mortalitet på 12% og en 3-års overlevelse på rundt 50 % i en stor nederlandsk kohort (Olthof et al., 2023), men er sterkt påvirket av seleksjon. En stor meta-analyse oppgir 90-dagers mortalitet på 6 % (van Keulen et al., 2023). Ablasjonsbehandling kan være aktuelt hos enkelte pasienter med små lesjoner (Masoud et al., 2023).
Lymfadenektomi i leverhilus anbefales (Bagante et al., 2015; Bridgewater et al., 2014; Greenblatt et al., 2011). Ved venstresidige svulster er det tidvis tidlig lymfeknutemetastasering til ventrikkelens minorside og dette kvalifiserer alene ikke til M1-sykdom etter UJCC versjon 8. Den mest kraniale av de retropankreatiske lymfeknutene har sannsynligvis prognose som tilsvarer M1.
Multifokalitet ved intrahepatiske kolangiocarcinomer
Multifokalitet er spesielt utfordrende. Det er ikke åpenbart om dette representerer multiple primærsvulster eller om alt er et uttrykk for intrahepatisk metastasering (Weber et al., 2015). Det er naturlig å oppfatte satellitt i annet segment enn primærtumor som metastase, og noen anser enhver multifokal tumor som et signal på inoperabilitet (Abou-Alfa et al., 2015). En stor kohortstudie av vestlige pasienter resecert for multifokal (>1) intrahepatisk kolangiocarcinom viste akseptabel overlevelse hos selekterte grupper. Faktorer assosiert med tidlig residiv og kort sykdomsspesifikk overlevelse var >2 tumores, lymfeknutemetastaser og R1-reseksjon (Buettner et al., 2019). Det ble imidlertid sett noen 5-års overlevere, spesielt i gruppen med bare to tumores. En ny meta-analyse bekrefter dette inntrykket (Jansson et al., 2023). Uansett må multiple tumores anses som et svært negativt prognostisk tegn (Moustafa et al., 2020), og preoperativ kjemoterapi bør vurderes. Spesielt gjelder dette ved multifokalitet over mer enn ett segment (Conci et al., 2018). Reseksjon av multifokalt intrahepatisk kolangiocarcinom bør vurderes strengt opp mot operativ risiko og gevinst, og ideelt sett kun gjøres i protokoll.
Anbefaling:
- Intrahepatisk kolangiocarcinom med multifokalitet (intrahepatiske metastaser, satellitter, flere primærsvulster) oppfattes som lokalavansert, og reseksjon anbefales ideelt sett innenfor studieprotokoll selv der det ikke foreligger manglende teknisk resektabilitet.
Kirurgi ved perihilære kolangiocarcinomer
Målet med kirurgi er å oppå en R0-reseksjon da flere studier tyder på at prognosen etter en R1 reseksjon er nesten like dårlig som for de ikke-resecerte. Nyere japanske studier viser at denne forskjellen ikke er målbar der det foreligger regionale metastatiske lymfeknuter (Hosokawa et al., 2023).
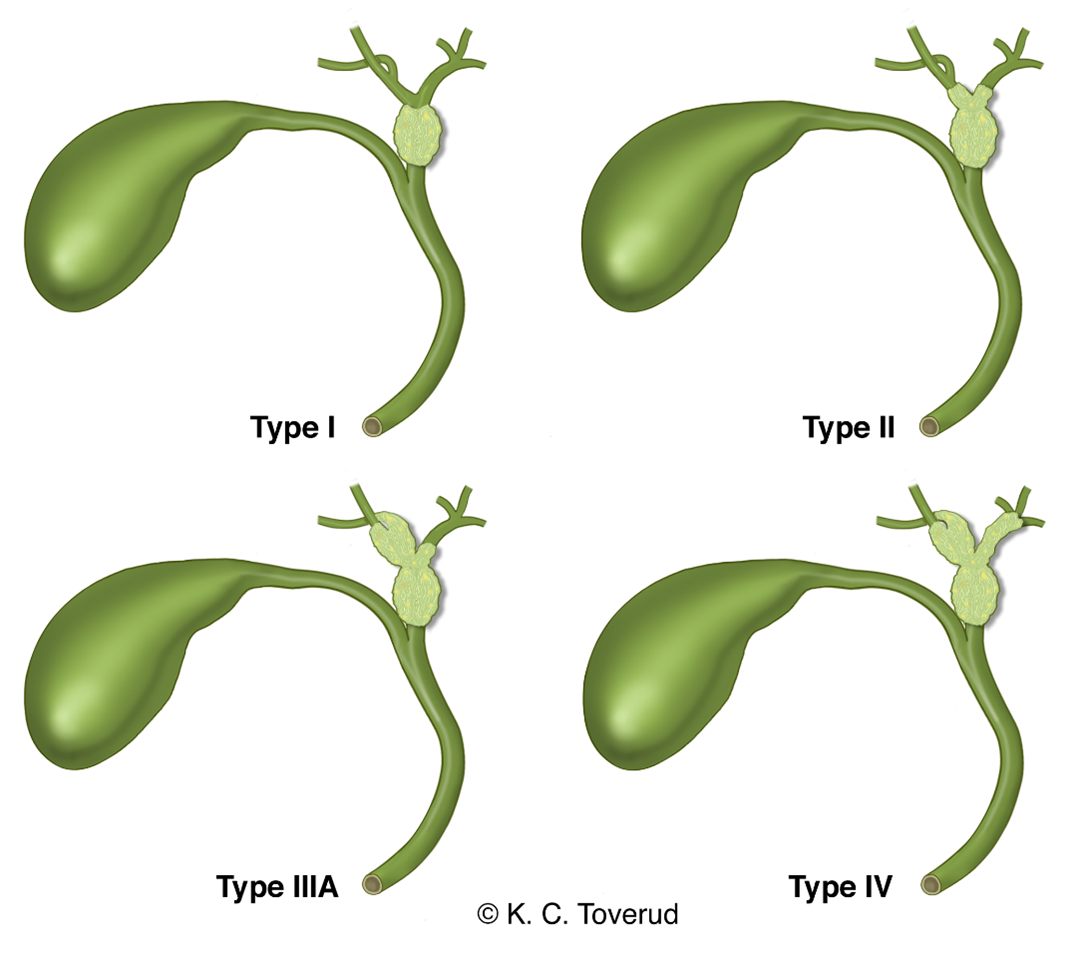
Resektabilitetsvurdering er ofte vanskelig og kan tidvis ikke avgjøres før eksplorasjon. Høyre leverarterie og portvene forløper rett bak gallegangens konfluens og dette gjør at disse hyppig er affiserte selv ved svulster som primært følger venstre gallegang. Bismuth-Corlette-klassifikasjonen har tradisjonelt vært enerådende, men gir ikke adekvat grunnlag for å bedømme resektabilitet eller overlevelse. Bismuth-Corlette type IV (2. ordens affeksjon av galleveier bilateralt) ble tidligere klassifisert som ikke-resektabel sykdom, men dette er ikke holdbart i dag (Ebata et al., 2018) selv om R1-raten må forventes å være høy. Ingen vestlige sentra har publisert serier som tilsvarer mer enn én reseksjon for perihilært kolangiocarcinom per måned.
Det er etter hvert betydelig dokumentasjon på at portvenerekonstruksjon for å oppnå resektabilitet har akseptabel morbiditet (Schimizzi et al., 2018; van Vugt et al., 2018). Rekonstruksjon av arteriesiden medfører mye høyere komplikasjonsrate, og er i utgangspunktet ikke indisert (der det samtidig skal gjøres formell leverreseksjon) (van Vugt et al., 2018). Bilateral arterieaffeksjon og portveneaffeksjon med kontralateral lobær atrofi signaliserer inoperabilitet.
Anbefaling:
- Volumekspanderende tiltak er anbefalt ved FLR < 30 %. God tilvekst fordrer at FLR allerede er adekvat drenert. Ved volum over 30 % uten adekvat/sikkert drenert FLR, må volumekspansjon vurderes individuelt.
Anbefaling:
- Drenasje av galleveier skal gjøres ved FLR < 50 %, og da kun av FLR. Drenasje av kontralaterale lever (som planlegges resecert) øker komplikasjonsrisikoen og ødelegger muligheten til å vurdere FLRs funksjon.
Anbefaling:
- Bilateral affeksjon av 2. ordens galleveier utelukker ikke R0-reseksjon.
Anbefaling:
- Portveneaffeksjon utelukker ikke reseksjon hvis portvenen kan rekonstrueres. Affeksjon av arterie til gjenværende lever vil vanligvis utelukke reseksjon.
Selv ved moderne radiologisk utredning påvises ikke-resektabel sykdom ved laparoskopi/laparotomi hos omtrent en tredjedel, og 20–30 % av pasienter operert med antatt R0 reseksjon har allikevel positiv margin (R1) (Mansour et al., 2015).
Reseksjon: Standard er formell leverreseksjon tilstrekkelig for å oppnå R0 med segment I og ekstrahepatiske galleveier samt lymfadenektomi i hilus (Hartog et al., 2016). Det er ikke dokumentert at lever- eller pankreasreseksjon øker overlevelsen der man kan sikre frie marginer ved reseksjon av tumor nedenfor konfluens (noen Bismuth-Corlette I eller II med veldig lav deling) (Kwon et al., 2014).
Arterieaffeksjon: Det er rimelig enighet ved vestlige sentra om at risikoen ved arterierekonstruksjon uten dokumentert overlevelsesgevinst ikke rettferdiggjør reseksjon (Hartog et al., 2016; van Vugt et al., 2018). Det er naturlig å vurdere dette noe annerledes hvis det ikke gjøres leverreseksjon (noen lave svulster).
Frysesnitt av gallegangsavsetning: har tradisjonelt vært anbefalt og ytterligere reseksjon kan tidvis resultere i R0. Det er dog ikke bevis for at bruk av frysesnitt eller ytterligere reseksjon forbedrer overlevelse med mindre markant større reseksjon kan utføres (Mantel et al., 2016).
Lymfadenektomi: Lymfatisk vev i leverhilus fjernes sammen med ekstrahepatisk gallegang.
Anbefaling:
Affeksjon av lymfeknuter utenfor leverligamentet tilsvarer ikke-regional lymfeknutemetastasering, og gir - i likhet med paraaortale og portocavale lymfeknuter - prognose som ved metastaser. Reseksjon anbefales ikke.
Kirurgi ved distale kolangiocarcinomer
Resektable distale kolangiocarcinomer går klar av gallegangenes konfluens. De opereres derved uten leverreseksjon, men med ekstrahepatiske galleveier, galleblære og regional lymfeknutehøst. For svulster som strekker seg ned i den intrapankreatiske delen av koledochus vil overgangen mot periampullære tumores og pankreastumor være vanskelig radiologisk, og utredning/reseksjonsvurdering vil oftest tilsvare tilsvarende vurdering for tumor i caput pankreatis.
Levertransplantasjon
Levertransplantasjon for ikke-resektabelt intrahepatisk kolangiocarcinom vurderes i ny protokoll (TESLA 1). Det skal foreligge stabil sykdom under kjemoterapi (6 mnd.) og ha gått minst 12 måneder fra diagnose. Det kan ikke foreligge noen form for ekstrahepatisk sykdom (inkludert lymfeknuter). Ikke-resektabelt residiv etter tidligere kirurgi (R0N0) kan i noen tilfeller vurderes gitt stabil sykdom under kjemoterapi (Oslo universitetssykehus, 2020). Lenke: TESLA1: Levertransplantasjon hos pasienter med ikke-operabel kreft i gallegangene i leveren - Oslo universitetssykehus HF (oslo-universitetssykehus.no)
Levertransplantasjon for ikke-resektable perihilært kolangiocarcinom vurderes i ny protokoll (TESLA 2). Det skal foreligge lokalisert sykdom, stabil under kjemoterapi i 10 måneder og påfølgende strålebehandling og ikke foreligge noen form for ekstrahepatisk sykdom (inkludert lymfeknuter). Det skal ha gått minst 12 måneder fra diagnosen (Oslo universitetssykehus, 2021). Lenke: TESLA2: Levertransplantasjon hos pasienter med kreft i gallegangene utenfor leveren - Oslo universitetssykehus HF (oslo-universitetssykehus.no)
Kirurgi ved galleblærekreft oppdaget in situ
All radiologisk påvist galleblærekreft må antas å være minst T1b.
- T1b: Standard kolecystektomi med regional lymfeknutehøst. Hvis tumor er i berøring med leverbundet del av galleblæren skal leverbrem tas med.
- T2a: Standard kolecystektomi (uten leverbrem), men med regional lymfeknutehøst.
- T2b: Utvidet kolecystektomi inklusive leverbrem fra Sg IVb/V og regional lymfeknutehøst.
- T3: Som T2b, samt med andre affiserte organdeler. Innvekst i duodenum/colon er ikke nødvendigvis assosiert med N+/M+-status og utelukker ikke reseksjon, selv om prognosen er dårlig.
- T4: Langtidsoverlevelse etter formell leverreseksjon, med reseksjon av kar og ekstrahepatiske galleveier, er anekdotisk og morbiditeten meget høy. Det anbefales derfor ikke reseksjon. Det er naturlig å revurdere situasjonen hvis det tilkommer markant og langvarig respons på kjemoterapi.
- T1b og høyere stadium:
- Ductus cysticus settes av flush i ductus hepatikus. Ved tumor i infundibulum eller annen mistanke om utstrekning til ductus, vurderes frysesnitt av reseksjonsranden mtp. reseksjon av ekstrahepatiske galleveier.
- Lymfeknuter fjernes i leverhilus kranialt for pankreas og medialt til vena coronaria/trunkus coeliakus.
Tykkelsen på leverbrem (der det er anbefalt) er ikke avgjørende, men fri margin er avgjørende (Kwon et al., 2020). Minst 2 cm er rettledende for å unngå tumorkontakt/perforasjon. Formell segmentreseksjon er ikke nødvendig (Aloia et al., 2015). Sannsynligvis er det ikke gevinst av leverreseksjon der tumor utelukkende er lokalisert til peritonealkledd/fri del av fundus/corpus (Lee et al., 2015).
Mistanke om galleblærekreft under kolecystektomi
Dersom det ved kolecystektomi mistenkes galleblærekreft bør inngrepet avbrytes og pasienten henvises til senter med leverkirurgisk kompetanse. Kolangiografi, tumorbiopsi og perforasjon bør unngås.
Anbefaling:
- Ved intraoperativ mistanke om galleblærekreft bør inngrepet avbrytes og pasienten henvises til senter med leverkirurgisk kompetanse.
Anbefaling:
- Galleblærekreft ansees ikke resektabel hvis det foreligger fjernmetastaser eller maligne lymfeknuter utenfor leverhilus, eller der det er infiltrasjon av portvene eller leverarterie.
Kirurgi ved galleblærekreft oppdaget ved histologisk undersøkelse etter kolecystektomi
Galleblærekreft som oppdages ved histologisk undersøkelse etter kolecystektomi kalles også insidentell galleblærekreft (etter engelsk: «incidental gall bladder cancer»).
Pasientene bør utredes for eventuell re-reseksjon ved HPB-avdeling. Histologi bør revurderes av patolog med spesialkompetanse for å klarlegge T-stadium og reseksjonsmargin i ductus cysticus og mot leverbundet flate. Tilleggsutredning gjøres med CT-thorax/lever (3‑fase)/abdomen/bekken, evt. MRCP og blodprøver inkl. CA 19-9, CEA. Da galleblærekreft ofte synes godt på PET kan dette være nyttig for å utelukke disseminert sykdom ved T2+ eller evt. støtte avgjørelsen om å avstå fra ny kirurgi ved T1b. Ved PET kort tid etter primærinngrep kan lokal inflammasjon postoperativt være en feilkilde.
Målet er R0-reseksjon. Formell reseksjon av lever eller gallegang er kun indisert for å oppnå R0. Der det ved primærinngrepet er tilkommet perforasjon eller tumorskade, eller det foreligger andre klart negative prognostiske faktorer og man må anta at risiko for peritoneal utsæd er stor, kan det vurderes å legge inn en observasjonstid før ny radiologisk staging og eventuell re-eksplorasjon. Målet her er å unngå laparotomi uten gevinst (okkult utsæd) (Qadan et al., 2016). Prognosen er i all hovedsak bestemt av tumorbiologi – ikke av ventetid for re-eksplorasjon.
Pasienter med radiologisk (inkludert PET) sterk mistanke om maligne lymfeknuter i hilus kan vurderes for kjemoterapi før ny radiologisk staging og eventuell re-reseksjon.
Basert på histologisk T-stadium i resektatet fra kolecystektomien:
- BilIn-III/CiS/T1a: Ingen ytterligere tiltak (det samme gjelder dermed BilIN I–II).
- T1b: Gevinsten ved re-reseksjon er usikker hvis PET-CT er negativ. Individuell avgjørelse (Søreide et al., 2019).
- T2 eller T3: Re-reseksjon, hvis ikke kontraindisert (AT) eller avansert sykdom: Cysticusplate med leverbrem reseceres. Hos pasienter der man er sikker på at tumor er beliggende utelukkende i fri, serosakledd del av fundus/corpus, kan det vurderes om leverreseksjon kan fravikes, men kunnskapsgrunnlaget for dette er mangelfullt (Lee et al., 2015; Qadan et al., 2016).
- Lymfeknuter i ligamentet fjernes. Ikke indisert med ytterligere lymfadenektomi (Qadan et al., 2016).
Innledende eksplorativ laparoskopi vurderes ved T3+ tumor og hvis det var perforasjon under kolecystektomien. Trokarportene trenger ikke reseceres (Aloia et al., 2015; Qadan et al., 2016).
Anbefaling:
- Pasienter med insidentell galleblærekreft bør vurderes ved HPB-senter med tanke på re-reseksjon eller kjemoterapi.